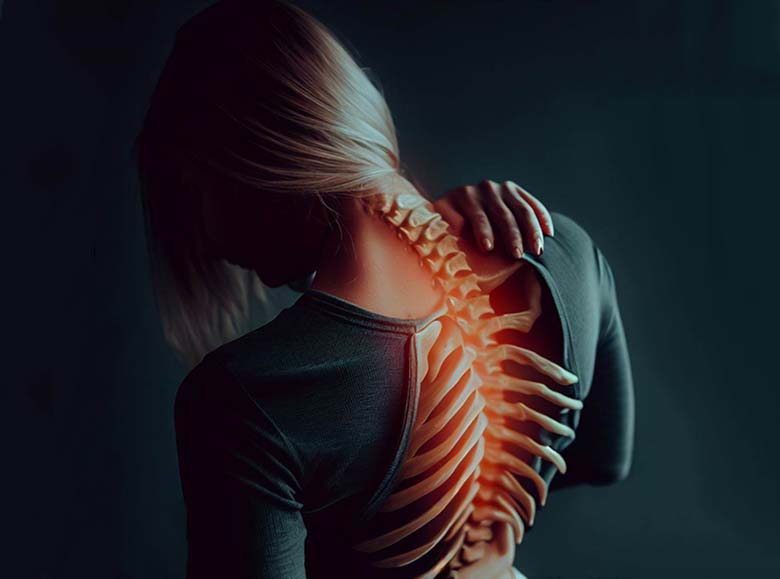
קשחת חוליות מה גורם לכך? דלקת חוליות מקשחת (אנקילוזינג ספונדיליטיס) היא מחלה דלקתית כרונית, אוטואימונית. הפרעה זאת פוגעת בעמוד השדרה ובמפרקים כגון כלוב הצלעות ומפרקי הירך וכן באיברים פנימיים כגון מערכת העיכול, עיניים ועוד. תסמיני המחלה עשויים להיות קלים ואפיזודיים אך עלולים גם להיות קשים ומתמשכים. בין התסמינים השכיחים ביותר של מחלה זאת נציין כאבים והגבלות תנועה קשות.
עדיין לא ברור מה הגורם להתפתחות הפרעה זאת שפוגעת בעיקר בגברים בגיל ביניים. בין יתר ההשערות שהועלו נציין גורמים סביבתיים, גורמים גנטיים, שילוב של מספר גורמים ועוד. אבחון של קשחת חוליות מתבסס על מידע שמופק מהמפגש שלנו עם החולה. המידע יכלול הכרת תסמיני החולה ורקעו הבריאותי, ממצאי הבדיקה הגופנית ובדיקות הדימות והמעבדה. לא ניתן לרפא קשחת חוליות אבל אפשר להאט את התקדמותה ולהפחית את חומרת התסמינים. עיקר הטיפול בקשחת חוליות הוא תרופתי. כירופרקט יכול להפחית כאב, לשפר את טווחי התנועה ואת היציבה.
קשחת חוליות מה גורם לכך – רקע
קשחת חוליות (Ankylosing Spondylitis -AS), או כחלק מהספקטרום של ספונדילוארתריטיס צירית (axial spondyloarthritis), היא מחלה דלקתית כרונית של עמוד השדרה והסקרואיליאק, המאופיינת בכאב גב דלקתי, נוקשות, ובהמשך גם בשינויים מבניים ואיחוי חוליות. למרות שהמחלה מוכרת כבר עשרות שנים, הגורמים המדויקים להתפתחותה עדיין אינם ברורים לחלוטין, והממצאים מצביעים על שילוב מורכב של גורמים גנטיים, סביבתיים, חיסוניים ומכניקיים (Zhu, 2019; Kim, 2023).
במאמר זה נסקור בצורה מעודכנת ויסודית את הגורמים הידועים והמשוערים להתפתחות קשחת חוליות -מהגנטיקה (ובעיקר HLA-B27), דרך מעורבות מערכת החיסון וציר IL-23/IL-17, דרך המיקרוביום במעי והשפעת העישון, ועד לתפקיד העומסים המכנית, ההורמונים והסביבה.
מרכיב גנטי חזק -אך לא בלעדי
HLA-B27 -הגן המפורסם ביותר בקשחת חוליות
הקשר בין קשחת חוליות לבין האנטיגן HLA-B27 מוכר כבר עשורים, ונחשב לאחד הקשרים החזקים ביותר בין גן יחיד לבין מחלת מפרקים. הערכות עדכניות מצביעות על כך ש-HLA-B27 אחראי לכ־20%-30% מהתורשתיות של המחלה (Chen, 2017; Kenyon, 2022).
עם זאת, חשוב להדגיש שני נתונים קריטיים:
- רוב חולי אנקילוזינג ספונדיליטיס הם HLA-B27 חיוביים
- אבל רק כ־1%-5% מנשאי HLA-B27 באוכלוסייה אכן יפתחו קשחת חוליות (Zormpa, 2025).
משמעות הדבר היא שהגן הזה חיוני כ"קרקע פוריה", אך אינו מסביר לבדו את התחלואה. מחקרים משפחתיים מראים שגם בין נשאי HLA-B27, קרבה משפחתית לחולה מעלה באופן חד את הסיכון -עד פי 16 בקרובים מדרגה ראשונה (Zhu, 2019; Kavadichanda, 2021).
גנים נוספים -הרבה מעבר ל־HLA-B27
מחקרי GWAS זיהו כיום עשרות וריאנטים גנטיים נוספים הקשורים לV,P,JU, אנקילוזינג ספונדיליטיס, בעיקר במסלולים חיסוניים:
- ERAP1/ERAP2 -אנזימים המשתתפים בעיבוד פפטידים והעמסתם על מולקולות HLA. קומבינציות מסוימות של ERAP1 עם HLA-B27 מגבירות את הסיכון למחלה (Chen, 2017; Kenyon, 2022).
- IL23R, IL12B, TYK2 -גנים המווסתים את ציר IL-23/IL-17, ציר מרכזי בהפעלת תאי Th17 ותאי מערכת חיסון מולדת (Tsukazaki, 2020).
- גנים במסלול NF-κB, במסלולי ציטוקינים נוספים, ובבקרה על התגובה המולדת והנרכשת (Kenyon, 2022; Zormpa, 2025).
צירוף הממצאים תומך בכך שקשחת חוליות היא מחלה בעלת "עומס גנטי" גבוה -אך רב־גני, כאשר HLA-B27 הוא שחקן מרכזי אך לא יחיד (Jain, 2020; Hazra, 2024).
מה עושה HLA-B27 בפועל? -היפותזות מרכזיות
למרות עשרות שנות מחקר, עדיין אין תשובה אחת מוסכמת לשאלה איך HLA-B27 תורם בפועל להופעת המחלה. כמה מנגנונים הוצעו, וסביר להניח שכולם תורמים במידה מסוימת (Colbert, 2014; Chen, 2017).
היפותזת הפפטיד הארתרוגני
HLA-B27 הוא מולקולה מציגה אנטיגן. לפי היפותזה זו, וריאנטים מסוימים של HLA-B27 מציגים פפטידים "חריגים" -למשל שמקורם בחיידקי מעי -הדומים מספיק לחלבוני מאכסן כדי לגרום לתגובה אוטו־אימונית (Zhu, 2019).
קיפול לקוי (misfolding) ועקה של הרטיקולום האנדופלזמטי
מחקרים הראו ש-HLA-B27 נוטה לקיפול לקוי ולהיווצרות דימרים והצטברות ב-ER, מצב היוצר עקת ER ומפעיל תגובת "חלבון מקופל־ביתר" (UPR) (Colbert, 2014; Colbert, 2013).
עקה זו יכולה:
- לשנות את ביטוי הציטוקינים (למשל לעודד ייצור IL-23).
- להשפיע על תפקוד מקרופגים ותאים דנדריטיים.
- ולהטות את התגובה החיסונית לכיוון פרו־דלקתי (Ambarus, 2018; Tsukazaki, 2020).
מחקרי מודל בעכברים וחולדות טרנסגניות ל-HLA-B27 הראו שאכן התקבלה תמונה של עקה ב-ER, דלקת במעי ובמפרקים, ועלייה בציטוקינים כגון IL-17 ו-IL-23 (Navid, 2024; Song, 2022).
דימרים על פני התא וקישור ל-NK/T
HLA-B27 יכול ליצור דימרים של שרשרת כבדה (heavy chain homodimers) על פני התא, המוכרים על־ידי קולטנים של תאי NK ותאי טי (T ) (Zhu, 2019). דימרים אלה עשויים לשנות את האיזון בין איתות מעכב ומפעיל במערכת המולדת, ולתרום להפעלת יתר כרונית. לסיכום חלק זה: HLA-B27 אינו "מתג יחיד" אלא חלק מרשת מורכבת של הצגת אנטיגן, קיפול חלבונים, תגובת עקה וצמתים של מערכת החיסון.
מערכת החיסון וציר IL-23/IL-17
אחד המאפיינים החשובים של קשחת חוליות (אנקילוזינג ספונדיליטיס) הוא התפקיד המרכזי של ציר IL-23/IL-17. טיפול ביולוגי המעכב IL-17A (כמו secukinumab) או מסלול קשור הוכיח יעילות קלינית, מה שמחזק את החשיבות הפתוגנטית של הציר הזה (Kim, 2023; Tsukazaki, 2020).
מחקרים מצאו:
- רמות מוגברות של IL-17 ו-IL-23 בדם ובנוזל מפרקי אצל חולי אנקילוזינג ספונדיליטיס לעומת בריאים.
- קשר בין רמת IL-17 לבין מדדי פעילות מחלה (Lobiuc, 2025).
- מעורבות תאי Th17, תאי T γδ, ותאי innate lymphoid מסוג 3 המייצרים IL-17/IL-22, בעיקר באזורי אנתזיס ומעי (Song, 2022).
Tsukazaki וחב' מציעים מודל שבו עקה ב-ER, שינויים במיקרוביום וגנטיקה במסלולי IL-23R ו-TYK2 מובילים ל"אקטיבציה יתר" של ציר IL-23/IL-17, וכך נוצרת דלקת כרונית באנתזיס ובעמוד השדרה (Tsukazaki, 2020).
המעי והמיקרוביום -"המפרק מתחיל בבטן"
דיסביוזיס של המיקרוביום במעי
בעשור האחרון נצברו עדויות חזקות לשיבוש במאזן חיידקי המעי (dysbiosis) בחולי אנקילוזינג ספונדיליטיס. סקירה שיטתית ומטה־אנליזה עדכנית שכללה 47 מחקרים מצאה ירידה מובהקת בעושר ובגיוון המיקרוביום אצל חולי AS לעומת בריאים (Su, 2024).
ממצאים חוזרים כוללים:
- ירידה בחיידקים מייצרי בוטיראט, במיוחד Faecalibacterium prausnitzii, בעלי השפעה אנטי־דלקתית מוכרת (Min, 2023).
- שינויים בהרכב המיקרוביום שמייחדים אנקילוזינג ספונדיליטיס מחולי IBD, למרות חפיפה חלקית; לדוגמה, העשרה של סוגים מסוימים העלולה להוות "טריגר משותף" (Sternes, 2022).
קשר בין HLA-B27 למיקרוביום
במודלים של חולדות טרנסגניות ל-HLA-B27 נמצא שמחלה דמוית אנקילוזינג ספונדיליטיסמתפתחת רק בנוכחות מיקרוביום -כאשר בעלי חיים גדלים בתנאי סטריליים (germ-free) המחלה כמעט ואינה מתפתחת (Song, 2022). מחקרי בני אדם מצאו כי וריאנטים של HLA (כולל HLA-B27) קשורים לשינויים ייחודיים בהרכב המיקרוביום במעי, גם באנשים בריאים (Vallier, 2023; Xu, 2019).
המודל המוצע:
- גנטיקה (למשל HLA-B27) משנה את אינטראקציית מערכת החיסון-מיקרוביום.
- מיקרוביום "דלקתי" יותר מגביר חדירות מעי ומעודד חדירת אנטיגנים/חיידקים למוקדי אנתזיס.
- תאי מערכת החיסון המופעלים במעי נודדים למפרקים ולעמוד השדרה וממשיכים לייצר ציטוקינים (IL-17, IL-23), וכך נוצרת דלקת מערכתית (Song, 2022; Lobiuc, 2025).
עישון, טיפול ביולוגי והמיקרוביום
Zhang וחב' הראו שחולי אנקילוזינג ספונדיליטיס מעשנים מציגים שונות נמוכה יותר במיקרוביום, ושעישון משנה את תגובת המיקרוביום לטיפול בנוגדי (TNF-α) (Zhang, 2020). מטה־ניתוח עדכני מצא שגם טיפול ביולוגי וגם עישון משנים את הרכב המיקרוביום באופן מורכב, מה שמדגיש את החשיבות של אינטראקציה בין גנטיקה, טיפול וסביבה במעי (Yang, 2025).
גורמים סביבתיים ואורח חיים
עישון
עישון הוא אחד מגורמי הסיכון הסביבתיים הבולטים שנקשרו לV,P,J, אנקילוזינג ספונדיליטיס:
- הוא מגביר סיכון להתפתחות המחלה.
- מחמיר את פעילותה ואת קצב התקדמות הנגעים המבניים.
- מפחית את תגובת המטופלים לטיפול ביולוגי (Hwang, 2021; Hazra, 2024).
סקירות עדכניות מדגישות שעישון פועל כנראה דרך מספר מנגנונים: עידוד דלקת מערכתית, שינוי במיקרוביום במעי, פגיעה באנדותל, והחמרת עקה חמצונית (Farran, 2022; Benucci, 2025).
זיהומים וחיידקי מעי ספציפיים
היסטורית, הועלתה השערה לגבי תפקיד חיידקי Klebsiella pneumoniae כמחוללים אפשריים, על סמך דמיון בין אנטיגנים חיידקיים לפפטידים המוצגים על-ידי HLA-B27 (Zhu, 2019). בעוד שהקשר הישיר ל-Klebsiella נותר שנוי במחלוקת, סקירות עדכניות מסכימות כי זיהומים במערכת העיכול והשתן, ושינויים חריפים-כרוניים במיקרוביום, יכולים לשמש כטריגר דלקתי בחולים בעלי נטייה גנטית (Farran, 2022; Song, 2022).
תזונה, השמנה וזיהום אוויר
המחקר בנושא תזונה והתפתחות אנקילוזינג ספונדיליטיס עדיין בראשיתו, אבל יש עדויות לכך שתזונה עתירת שומן רווי וסוכר, והשמנה בטנית, קשורות להחמרת פעילות מחלה ולדלקת מערכתית מוגברת (Hwang, 2021; Benucci, 2025).
סביבת חיים עירונית עם זיהום אוויר גבוה נקשרה בעלייה בסיכון למחלות דלקתיות שונות; ראיות חדשות מציעות שזיהום אוויר עלול להיות אחד הגורמים הסביבתיים המשתתפים גם בהתפתחות ספונדילוארתריטיס, אם כי הראיות עדיין מוגבלות (Benucci, 2025).
עומס מכני, אנתזיס ו"נקודות החיבור"
קשחת חוליות (אנקילוזינג ספונדיליטיס) מאופיינת בדלקת ב־אנתזיס -אזורי חיבור גיד/רצועה לעצם (במיוחד בעמוד השדרה והסקרואיליאק). עובדה זו הובילה להשערה שתפקיד מרכזי יש לעומס מכני ולהפרעה מיקרו־טראומטית מתמשכת (Jain, 2020; Kim, 2023).
מודל "העומס המכניקי" מציע:
עומס חוזר גבוה על האנתזיס (למשל בעבודה פיזית, ספורט עצים או יציבה מוקפדת) גורם למיקרו־פציעות. באנשים עם נטייה גנטית, ריפוי המיקרו־פציעות מלווה בדלקת יתר, הפעלה לא תקינה של מערכת החיסון, ובהמשך גם בהשקעת עצם ויצירת זיזים (syndesmophytes) (Venerito, 2023; Singh, 2025).
מחקרים מבוססי MRI מראים שבמקומות החשופים לעומס מכני -כמו החלק הקדמי של חוליות, חיבור גיד אכילס, fascia plantaris -יש שכיחות גבוהה של אות דלקתי בחולי AS ו-axSpA, גם בשלבים מוקדמים של המחלה (Kim, 2023).
- ההשפעה אינה חד־כיוונית: פעילות גופנית מתונה ומבוקרת יכולה לשפר כאב ותפקוד, בעוד עומסים קיצוניים, חוזרים ולא מבוקרים עשויים לשמש טריגר בחלק מהחולים.
מין, הורמונים וגיל
קשחת חוליות ה"קלאסית" הוגדרה במשך שנים כמחלה "גברית", עם יחס גברים:נשים של כ־3:1 במופעי אנקילוזינג ספונדיליטיס רדיוגרפיים. בשנים האחרונות, עם ההכרה בצורות לא־רדיוגרפיות (nr-axSpA), התברר שהפער קטן יותר, במיוחד בשלבים מוקדמים, אך עדיין קיימים הבדלים בין המינים (Hwang, 2021; Hazra, 2024).
הסברים אפשריים:
- הורמוני מין (טסטוסטרון, אסטרוגן) משפיעים על המסלולים החיסוניים הרלוונטיים, על צפיפות עצם ועל תגובת האנתזיס לעומס.
- גברים נוטים להראות יותר שינויים מבניים רדיוגרפיים (איחוי חוליות), בעוד אצל נשים לעיתים קרובות יותר דפוס של כאב ודלקת בלי איחוי מוקדם (Hwang, 2021).
גיל ההתחלה השכיח הוא בשנות העשרים-שלושים, אם כי המחלה יכולה להתחיל גם בגיל מאוחר יותר. המשמעות היא שגורמים סביבתיים לאורך הילדות והנעורים -זיהומים, תזונה, עישון מוקדם -עשויים להשפיע על סיכון ההתפתחות (Zhu, 2019; Hwang, 2021).
אינטראקציה גן-סביבה: לא "או-או" אלא "גם וגם"
סקירה שיטתית עדכנית של גורמי סיכון בהתפתחות אנקילוזינג ספונדיליטיס מסכמת שהמחלה היא תוצר של אינטראקציה מורכבת בין גנים, מיקרוביום, עומס מכני, מגדר וגורמי סביבה נוספים (Hwang, 2021).
אפשר לנסח מודל רב־שכבתי:
שכבה גנטית
HLA-B27 ומגוון גנים נוספים (ERAP1, IL23R ועוד) יוצרים "קרקע ביולוגית" של תגובה חיסונית שונה. (Chen, 2017; Kenyon, 2022; Zormpa, 2025).
שכבה מיקרוביאלית
שינוי בהרכב מיקרוביום המעי -אולי בעקבות דיאטה, זיהומים, אנטיביוטיקה או עישון -גורם לדלקת מעיתית תת־קלינית, לחדירות מוגברת ולייצור אנטיגנים וציטוקינים (Song, 2022; Su, 2024; Min, 2023).
שכבה מכנית
עומס יתר על אנתזיס בעמוד השדרה, אגן וגפיים גורם למיקרו־פציעות; "סביבת המפרק" הופכת דלקתית ומגייסת תאי מערכת חיסון "מחוממים" ממערכת העיכול (Venerito, 2023; Singh, 2025).
שכבה סביבתית-התנהגותית
עישון, תזונה עתירת שומן וסוכר, זיהום אוויר וסטרס כרוני מחזקים דלקת מערכתית ומעוותים את האיזון החיסוני (Farran, 2022; Benucci, 2025).
שכבה חיסונית
כל השכבות הללו מתכנסות לציר IL-23/IL-17 ותאי Th17/ILC3, וליצירת דלקת כרונית באנתזיס, במפרקים ובמפרקי הסקרואיליאק (Tsukazaki, 2020; Lobiuc, 2025). חשוב להבין: אין "גורם אחד" שבלעדיו לא תתפתח קשחת חוליות, אלא צירוף של נטייה גנטית ומספר "טריגרים" סביבתיים ומכנית, שיחד דוחפים את המערכת לכיוון מחלה.
מה עדיין לא ברור? מגבלות הידע הנוכחי
למרות ההתקדמות הגדולה, נשארו שאלות פתוחות:
מדוע רק חלק קטן מנשאי HLA-B27 מפתחים מחלה?
ייתכן שהסבר טמון בשילוב ספציפי של גנים נוספים, סוג המיקרוביום, מין, וסוגי חשיפה סביבתית.
מה התפקיד המדויק של כל רכיב במיקרוביום?
אנו יודעים שיש דיסביוזיס, אבל קשה להבחין בין "סיבה" ל"תוצאה", וטרם זוהו חיידקים ספציפיים שתפקידם הוכח סיבתית (Sternes, 2022; Su, 2024).
האם התערבות במיקרוביום (פרוביוטיקה, דיאטה, השתלת צואה) יכולה למנוע או לשנות מהלך מחלה?
נכון להיום אין הוכחות חזקות לכך, אם כי זהו תחום מחקר פעיל (Song, 2022; Lobiuc, 2025).
מדוע הדפוסים שונים בין גברים לנשים ובין קבוצות אתניות שונות?
כאן נדרש מחקר נוסף המשלב גנטיקה, הורמונולוגיה וסוציואקונומיה.
סיכום
קשחת חוליות (אנקילוזינג ספונדיליטיס) היא מחלה דלקתית כרונית מורכבת, שמקורותיה אינם "מפרקיים" בלבד. התמונה העדכנית של הגורמים להתפתחותה כוללת:
- נטייה גנטית חזקה, בהובלת HLA-B27 וגנים נוספים המעורבים בהצגת אנטיגן, עיבוד פפטידים ומסלולי ציטוקינים (Chen, 2017; Kenyon, 2022; Zormpa, 2025).
- מנגנוני קיפול לקוי ועקת ER ב-HLA-B27, היוצרים תגובה דלקתית מוגברת והפעלת ציר (IL-23/IL-17) (Colbert, 2014; Tsukazaki, 2020).
- מערכת חיסון מוטת Th17/IL-17, עם מעורבות תאי T ותאי מערכת חיסון מולדת באנתזיס, בעמוד השדרה ובמערכת העיכול (Song, 2022; Lobiuc, 2025).
- דיסביוזיס של מיקרוביום המעי, ירידה בחיידקים מייצרי בוטיראט ושינויים בהרכב החיידקים, אשר מתקשרים גם לנוכחות HLA-B27 וגם לדלקת מערכתית (Su, 2024; Min, 2023; Sternes, 2022).
- גורמים סביבתיים ואורח חיים, כמו עישון, זיהומים, תזונה, השמנה וזיהום אוויר, המשמשים כטריגרים או כמגבירים של דלקת (Hwang, 2021; Farran, 2022; Benucci, 2025).
- עומס מכני על אנתזיס, המביא למיקרו־פציעות חוזרות ולהפעלת יתר של מערכת החיסון באזורי חיבור גיד-עצם (Venerito, 2023; Singh, 2025).
- השפעות של מין, הורמונים וגיל, המעצבות את הביטוי הקליני ואת הסיכון לפתח מחלה (Hwang, 2021; Hazra, 2024).
המחלה נולדת, ככל הנראה, מהצטברות של "חוליות" רבות בשרשרת: גנטיקה, מעי, עמוד שדרה, אורח חיים וסביבה. הבנת כל אחת מן החוליות הללו מאפשרת לפתח טיפולים ממוקדים יותר -כמו עיכוב IL-17/IL-23 -אך גם מחזקת את ההבנה ששליטה בגורמי סיכון סביבתיים (ובעיקר הפסקת עישון, איזון משקל, תנועה ושמירה על בריאות מעי) עשויה להשפיע על מהלך המחלה, ובטווח הארוך אולי גם על הסיכון להתפתחותה באנשים בעלי נטייה גנטית.
References:
Chen, B., Li, J., He, C., Li, D., Tong, W., Zou, Y., Xu, W., & Yang, L. (2017). Role of HLA-B27 in the pathogenesis of ankylosing spondylitis. Molecular Medicine Reports, 15(4), 1943-1951.
Colbert, R. A. (2014). HLA-B27 misfolding and ankylosing spondylitis. Arthritis & Rheumatology, 66(11), 2721-2723.
Farran, Y., & Gossec, L. (2022). Environmental risks for spondyloarthropathies. Rheumatic Disease Clinics of North America, 48(4), 737-752.
Hazra, N., Khosla, J., & Brown, M. A. (2024). Unraveling ankylosing spondylitis: Exploring the genetic architecture and its clinical implications. The Lancet Rheumatology, 6(3), e210-e222.
Hwang, M. C., Ridley, L., & Reveille, J. D. (2021). Ankylosing spondylitis risk factors: A systematic literature review. Clinical Rheumatology, 40(7), 2543-2558.
Jain, N., Lam, N., & Garg, B. (2020). Current concepts in the pathogenesis of spondyloarthritis. Indian Journal of Rheumatology, 15(Suppl. 1), S31-S38.
Kavadichanda, C. G., Geng, L., & Brown, M. A. (2021). Spondyloarthritis and the human leukocyte antigen (HLA) class I. Frontiers in Immunology, 12, 601518.
Kenyon, M., Maksymowych, W. P., & Brown, M. A. (2022). The genetic backbone of ankylosing spondylitis: How knowledge of genetic susceptibility informs pathogenesis and disease management. Rheumatology International, 42(11), 1873-1885.
Kim, S. H., Kim, T. H., & Inman, R. D. (2023). Updates on ankylosing spondylitis: Pathogenesis and clinical features. Rheumatology and Therapy, 10(3), 423-445.
Lobiuc, A., et al. (2025). Gut microbiota and ankylosing spondylitis: From association to potential therapeutic target. Microbial Cell, 12(1), 1-17. (Microbial Cell)
Min, H. K., Sung, M., Kim, H. Y., et al. (2023). Identification of gut dysbiosis in axial spondyloarthritis and the impact of butyrate on inflammation. Frontiers in Immunology, 14, 1096565.
Navid, F., et al. (2024). CHOP-mediated IL-23 overexpression does not drive spondyloarthritis-like disease in HLA-B27 transgenic rats. Scientific Reports, 14, 12345.
Song, Z. Y., Zhang, Y. F., & Wang, R. (2022). Role of the microbiome and its metabolites in ankylosing spondylitis. Frontiers in Immunology, 13, 988485.
Sternes, P. R., De Filippis, F., Natividad, J. M., et al. (2022). Distinctive gut microbiomes of ankylosing spondylitis and inflammatory bowel disease patients. Arthritis Research & Therapy, 24, 256.
Su, Q. Y., Li, X., & Zhang, J. (2024). Gut microbiota dysbiosis in ankylosing spondylitis: A systematic review and meta-analysis. Frontiers in Cellular and Infection Microbiology, 14, 1376525.
Tsukazaki, H., & Kaito, T. (2020). The role of the IL-23/IL-17 pathway in the pathogenesis of spondyloarthritis. International Journal of Molecular Sciences, 21(17), 6401.
Vallier, M., et al. (2023). Characterisation of gut microbiota composition in patients with axial spondyloarthritis and its association with HLA-B27. RMD Open, 9(1), e002794.
Venerito, V., Lopalco, G., & Iannone, F. (2023). Beyond the horizon: Innovations and future directions in axial spondyloarthritis. Archives of Rheumatology, 38(2), 123-135.
Yang, L., Zhang, X., & Wang, Y. (2025). Dysbiosis of gut microbiota in ankylosing spondylitis patients: A comprehensive analysis. Journal of Inflammation Research, 18, 101-120.
Zhang, F., Ma, C., Zhang, B., et al. (2020). Dynamic changes in gut microbiota under the influence of smoking and TNF-α blocker in patients with ankylosing spondylitis. Clinical Rheumatology, 39(9), 2653-2661.
Zhu, W., He, X., Cheng, K., & Zhang, L. (2019). Ankylosing spondylitis: Etiology, pathogenesis, and treatments. Bone Research, 7, 22.
Zormpa, T., et al. (2025). The genetic background of ankylosing spondylitis and disease-associated risk variants. Journal of Clinical Medicine, 14(11), 3677.