מורטון נוירומה: אבחון וטיפול הנעשים מהר עשויים למנוע נזקים וכאבים כרוניים. בהפרעה בריאותית זאת סיב העצב שעובר בין עצמות המסרק בכף הרגל נפגע, נדלק ומתנפח. הגורם להתפתחות מורטון נוירומה הם לרוב עומסי יתר חוזרניים הנגרמים בגלל הליכות, ריצות ועמידות ממושכים. מלבד כאב בכף הרגל החולה הלוקה בתופעה התלונן על תחושות דגדוג ושריפה, הירדמות של האצבע ועוד. הפרעה בריאותית זאת בדומה להפרעות אחרות בכף הרגל נוטה להיעשות כרונית.
עיכוב באבחון ובהענקת טיפול מתאים מקשים מאוד על מלאכת הריפוי. ועל כן בכל מקרה של מורטון נוירומה אבחון וטיפול צריכים להיות הצעדים המיידים שלכם. כאבים בכף הרגל ותסמינים עצביים כגון נימול או תחושת שריפה מעלים חשד שמדובר במורטון נוירומה. עם זאת תסמינים אלה עלולים להתפתח גם בגלל הפרעות בריאותיות אחרות. ועל כן אבחון מדויק חשוב כדי לקבוע את אופן הטיפול המתאים.
מורטון נוירומה: אבחון וטיפול – רקע
מורטון נוירומה היא התעבות/דלקת של סיב העצב הבין־אצבעי (interdigital) בכרית כף־הרגל. דלקת זאת מתפתחת לרוב בין ראשי המסרק השלישי-הרביעי או השני-השלישי. הלחצים החוזרניים בעומס־נשיאה, הנעלה צרה או נעלי עקב, ועיוותים מבניים מגבירים חיכוך וגירוי לעצב עד להידלקותו.
תסמיני מורטון נוירומה כוללים כאב שורף, נימול, תחושת “אבנים בנעל” ולעיתים הקרנה לשתי האצבעות הסמוכות. אבחון וטיפול סמוך לתחילת התסמינים משפרים סיכויי היעלמות הכאב ומפחיתים סיכון לכרוניות ולניתוח (Hassouna, 2005; Wu, 1996). רוב המטופלים משתפרים עם שינוי הנעלה, תמיכה אורתוטית, ניהול עומסים וטיפולים ממוקדים. מיעוטם יידרשו להזרקות ולעיתים גם להתערבות כירורגית (Pace, 2010).
רקע ואפידמיולוגיה
כאב בכרית כף־הרגל (מטטרסלגיה) הוא תלונה שכיחה. מורטון נוירומה היא אחד הגורמים המרכזיים בתת־קבוצה זו, ושכיחה יותר בנשים בשנות ה־40-50 לחייהן (Hassouna, 2005). הסיבה לשכיחות גבוהה יותר אצל נשים אינה חד־משמעית, אך השערות כוללות צורת הנעלה (עקב צר/מחודד) ושונות ביומכאנית של קדמת כף־הרגל (Hassouna, 2005).
מציאות נוספת שיש לזכור: התרחבות עצבית בין־אצבעתית עשויה להופיע גם באוכלוסייה ללא תסמינים ולא כל ממצא הדמייתי מחייב טיפול (Symeonidis, 2012). מכאן החשיבות של קורלציה קלינית ואבחנה מבדלת, ולא רק אבחון מצילום או אולטרה סאונד. השכיחות של מורטון נוירומה תלויה במדידה:
היארעות (incidence) קלינית של מורטון נוירומה מוערכת:
- בכ-50.2 ל-100,000 גברים וב-87.5 ל-100,000 נשים לשנה באוכלוסייה הכללית. כלומר, זה נפוץ יותר בנשים בגיל העמידה.
“שכיחות” בהדמיה באנשים ללא תסמינים גבוהה בהרבה. מחקרי MRI/אולטרסאונד מצאו ממצאים תואמי נוירומה בכ-~33% ואף יותר בקרב מתנדבים א־סימפטומטיים. נתון זה מדגיש שממצא הדמייתי לבדו לא שווה לאבחנה קלינית. לכן: קלינית זו בעיה יחסית לא שכיחה, אך ממצאי הדמיה “דמויי נוירומה” יכולים להופיע גם בלי כאב.
פתופיזיולוגיה
בקדמת כף־הרגל, בין ראשי עצמות המסרק, עוברים ענפי העצב הדיגיטליים הפלנטריים בתוך מרווח הדוק יחסית. עומסי יתר חוזרניים כגון הליכה/ריצה על משטחים קשים, קפיצות, עמידה ממושכת, יחד עם הנעלה צרה או קשת לא מאוזנת, מעלים חיכוך וגזירה על העצב ועל הרקמות הסובבות. התגובה הביולוגית כוללת בצקת, פיברוזיס והתעבות מקומית (“נוירומה”). מורטון נוירומה מתבטאת בכאב נוירופתי, תחושת שריפה ודגדוג, ולעיתים תחושת “ניצוץ” בהעמסה מכוונת של המרווח (Hassouna, 2005; Wu, 1996). יש עדויות שדפוסי הנעלה מודרניים תרמו לעלייה בפתולוגיות קדמת כף־הרגל בהשוואה להליכה יחפה/מסורתית (Zipfel & Berger, 2007).
גורמים וגורמי סיכון
הגורם המדויק להתפתחות מורטון נוירומה אינו ברור כלל ועיקר. חוקרים סבורים שמדובר בגירוי מכני של אחד מענפי העצב הפלנטרי הדיגיטלי בעוברו בין עצמות המסרק. גירוי העצב נוצר בגלל הגורמים וגורמי הסיכון הבאים:
- הנעלה: עקבים גבוהים, חזית צרה (“שפיץ”), נעל קשיחה בלי מרחב אצבעות – מגבירים לחץ בין־מסרקי (Hassouna, 2005).
- עומסי יתר: ריצה/עמידה ממושכת, קפיצות, שינוי חד בעומס שבועי.
- מבנה כף־רגל: קשת גבוהה מאוד/שטוחה, בוהן קלובה (Hallux valgus), בהונות פטיש – משנים את חלוקת העומס (Hassouna, 2005).
- משקל עודף: מגביר כוחות דחיסה וגזירה בקדמת כף־הרגל.
- טראומה מקומית: “נחיתה על אבן”, מכה חוזרת – טריגר להתלקחות (Wu, 1996).
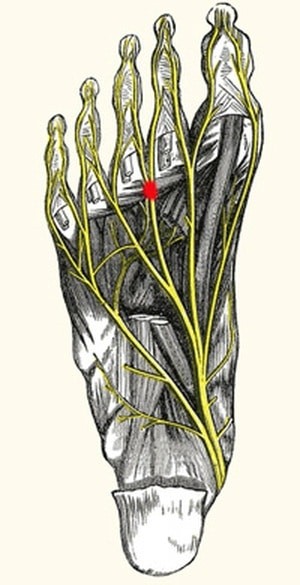
סימנים ותסמינים של מורטון נוירומה
תמונה קלינית טיפוסית כוללת:
- כאבים נוירופתיים בכרית כף־הרגל (ball of the foot), לעיתים “כאב שורף” או “תחושת גזירה”, שמוחמר בעמידה/הליכה, במיוחד עם נעל צרה או עם עקב.
- נימול/עקצוץ בשתי האצבעות שממסגרות את המרווח הפגוע.
- תחושת גוף זר/אבנים בנעל, עם הקלה מיידית בניעור הנעל או עיסוי קל.
- החמרה בלחיצה לרוחב קדמת כף־הרגל. לעיתים נשמע/נחוש קליק במניפולציה בין ראשי המסרק (Mulder’s sign).
- לרוב חד־צדדי; דו־צדדי נדיר יותר. התסמינים עשויים לנוע בין התקפים קצרים לכאב מתמשך היוצר הימנעות מפעילות.
אבחון של מורטון נוירומה
היסטוריה קלינית ממוקדת
בשלב הזה נברר את (Hassouna, 2005):
- משך הופעת התסמינים
- דפוס החמרה/הקלה
- סוגי נעלים
- עומסי פעילות
- היסטוריה של שינויי משקל/עבודה
- תסמינים נוירופתיים נלווים.
בדיקה גופנית
בשלב הזה נתבונן, נמשש ונניע את כף הרגך כדי:
- לאתר את המיקום עם הרגישות המרבית במרווח הבין־מסרקי החשוד.
- נבצע "סחיטה" לרוחב קדמת כף־הרגל (“squeeze”) עם שחזור נימול/כאב לרוחב שתי האצבעות הסמוכות.
- נחפש את Mulder’s sign: דחיסה מהצד עם לחץ מרווחילעיתים קליק מכאיב.
- הערכת הליכה/תנוחה: חיפוש עומס יתר קדמי, קריסה/רוחב קשת, טווחי מסרק־פלנגיאלי.
- סקר נוירולוגי: תחושה דיסטלית, כח אצבעות, שלילת מעורבות פרוקסימלית.
הדמיה
- אולטרסאונד: זמין, דינמי ומאפשר הדגמת גוש נוירומטי בין ראשי המסרק. רגיש במיוחד בידיים מיומנות (Fazal, 2012).
- MRI: שימושי כאשר האבחנה אינה חד־משמעית או לשלול פתולוגיה אחרת (שבר מאמץ, פרייבורג וכו’) (Fazal, 2012).
זכרו: ממצאים אקראיים של התעבות עצבית באוכלוסייה א־סימפטומטית אינם נדירים. לכן יש לשקלל קליניקה עם הדמיה (Symeonidis, 2012).
אבחנה מבדלת
כאבים בכף הרגל יכולים להתפתח בגלל סיבות רבות. טרם האבחון של מורטון נוירומה יש לבצע אבחנה מבדלת ולשלול גורמים אחרים שעלולים לגרום לתסמינים דומים ובכללם (Fuhrmann, 2005):
- מטטרסלגיה מכנית שאינה נוירומה
- דלקת בכרית השומן
- פרייבורג (נמק ראש מסרק)
- שבר מאמץ
- ססמואידיטיס
- תסמונת התעלה הטרסלית
- ציסטות וגידולים נדירים.
טיפול עצמי ראשוני
בימים/שבועות הראשונים, ובעיקר כשאין “דגלים אדומים”, ניתן לנקוט צעדים פשוטים שמפחיתים עומס וגירוי עצבי:
- החלפת נעליים: חזית רחבה (toe box), עקב נמוך, סוליה מרופדת וגמישה בקדמת כף־הרגל.
- תמיכות/רפידות: “metatarsal pad” או דום־מדורג להפחתת לחץ מרווחי.
- ניהול עומסים: הורדת זמנית של הליכות ארוכות/ריצה וכפיפה ממושכת על קדמת כף־הרגל; מעבר מדורג לפעילות דלת־עומס (אופניים/שחייה).
- משקל גוף: הפחתה מתונה משפרת חלוקת עומסים.
- חזרה מדורגת: גם לאחר שוך הכאב לשמור על זהירות 4-8 שבועות כדי לאפשר ריפוי רקמה (Hassouna, 2005).
טיפול שמרני מקצועי
שינוי הנעלה ואורתוטיקה
ההתערבות בעלת יחס עלות־תועלת הגבוה ביותר: נעל רחבה ומרופדת, סוליית רוקר במקרים מתאימים, ותמיכה מטרטרסלית שמפזרת עומסים מן המרווח הכואב. התאמה נכונה של מיקום ה־pad מעט לפני לראשי המסרק היא קריטית (Hassouna, 2005).
כירופרקטיקה/פיזיותרפיה ממוקדת
- חינוך וניהול עומסים: הדרכה קונקרטית למניעת “טריגרים” יומיומיים.
- טיפול ברקמות רכות: שחרור פאשיות קדמת כף־הרגל, גמישות מסרק־פלנגיאלית.
- שליטה וביו־מכניקה: אימון שליטה אצבעתית, פרופריוספציה של קדמת כף־הרגל, גיוס תנועתיות סובטלרית.
- שרשרת קינמטית: טיפול בחולשות/קשיחות פרוקסימליות (ירך, ליבה) המגבירות עומס קדמי.
- מכשור פיזיקלי: לעיתים נעשה שימוש בלייזר רך/אולטרסאונד טיפולי/גלי הלם כהתערבות משלימה בתקופת כאב חריף (Rattray & Ludwig, 2000).
גלי הלם חוץ־גופיים (ESWT)
מחקר אקראי כפול־סמיות הראה ש־ESWT עשוי להפחית כאב במורטון נוירומה לעומת פלסבו, במיוחד כחלק מתכנית שמרנית רב־מרכיבית (Fridman, 2009).
הזרקות
- סטרואידים: עשויים לספק הקלה קצר־בינונית, בעיקר בשלב דלקתי פעיל. יש לשקול תופעות לוואי מקומיות וחזרתיות (Hassouna, 2005).
- אלכוהול: הזרקה נוירוליטית מדורגת (לרוב סדרת הזרקות בהנחיית אולטרסאונד) יכולה לשכך כאב במקרים עמידיםאך כרוכה בסיכון כאב נוירופתי ודיסאסתזיות. הבחירה סלקטיבית (Wu, 1996).
קיימות גם טכניקות נוספות (קריותרפיה/גלי רדיו) במרכזים ייעודיים בבחירת מקרים קפדנית.
מתי לשקול ניתוח?
ניתן לשקול התערבות כירורגית במצבים הבאים:
- הטיפול השמרני המלא (כולל הנעלה/אורתוטיקה, ניהול עומסים, פיזיותרפיה/כירופרקטיקה, ולעיתים הזרקות) אינו מביא לשיפור מספק לאחר מספר חודשים.
שתי מטרות אפשריות בניתוח כוללות:
- דה־קומפרסיה (שחרור הרצועה הבין־מסרקית) או כריתת הנוירומה.
התוצאות לרוב טובות, אך לא נטולות סיכון (Pace, 2010). תופעות לוואי אפשריות כוללות:
- כאב מתמשך/הישנות.
- נוירומה “סטאמפ” או גדם נוירומה שהוא תוצאה של עצב המנסה להתחדש לאחר שנחתך או נפצע. העצב יוצר כדור בולבוסי ולא מאורגן של רקמת עצב, הנקרא גם "נוירומה טראומטית" או "נוירומה צלקתית".
- היפואסתזיה באצבעות הסמוכות.
- לעיתים הגבלת פעילות זמנית עד חודשים.
שיעורי הצלחה טובים מתוארים בסדרות אך גם שיעור לא זניח של כאב שארי (Pace, 2010). הבחירה בין גישה גבית/פלנטרית משפיעה על פרופיל ההחלמה והסיבוכים (Pace, 2010). לכן, ניתוח הוא מוצא־אחרון מושכל ולא קו ראשון.
קו־מנחה פרקטי לקבלת החלטות
שלב 1: אבחון קליני מדויק
קליניקה תואמת + בדיקה פיזית עם שחזור תסמינים; הדמיה באולטרסאונד או MRI כאשר יש ספק או כישלון טיפול ראשוני (Fazal, 2012; Symeonidis, 2012).
שלב 2: טיפול שמרני מובנה ל־8-12 שבועות
הנעלה רחבה, רפידה מותאמת למטרטרסל, ניהול עומסים, תרגול וייעול ביומכאניקה. לשקול שימוש בגלי הלם ESWT לפי צורך (Fridman, 2009).
שלב 3: הזרקות ממוקדות
בסימפטומים עמידים הזרקת סטרואידים/אלכוהול בהנחיית US, תוך הסבר מלא על יתרונות/סיכונים (Hassouna, 2005; Wu, 1996).
שלב 4: ניתוח
כישלון ממושך של שמרני/הזרקות או פגיעה משמעותית באיכות חיים/תפקוד. לבצע הערכה כירורגית, בחירת טכניקה מותאמת וציפיות שיקום ריאליות (Pace, 2010).
מניעת מורטון נוירומה
- בחירת נעליים: מרווח אצבעות נדיב, עקב מתון, סוליה בולמת זעזועים, התאמה לפעילות (הליכה ≠ ריצה).
- הדרגתיות בעומסים: העלאות נפח/עצימות של פעילות אירובית/ריצה – רק ב־10% לשבוע.
- מדרסים/תמיכות: במבנה קשת קיצוני, בוהן קלובה, או “אצבעות פטיש”- לשקול תמיכה להפחתת עומס מרווחי.
- ניהול משקל: כל ירידה משפרת חלוקת עומסים.
- היגיינת כף־רגל: גרביים מתאימים, ייבוש לאחר מקלחת, גזירת ציפורניים בטוחה – למניעת גורמי גירוי נוספים.
- מודעות לתסמינים: חזרת “ניצוצות/שריפה” בתחילת פעילות? עצרו, התאימו נעליים/רפידות, ושקלו ייעוץ מוקדם – אל תחכו לכרוניות (Hassouna, 2005).
שאלות נפוצות: תשובות קצרות
האם כל נוירומה דורשת MRI?
לא. כאשר הקליניקה אופיינית והתגובה לטיפול שמרני טובה, ניתן לוותר. MRI שמור למצבים לא ברורים או טרום־התערבות (Fazal, 2012).
האם הזרקת סטרואידים “מרפאה”?
לעיתים היא מפחיתה דלקת וכאב לתקופה ארוכה אך אינה “ממיסה” את הנוירומה. הזרקה מיועדת כגשר לשיקום ולניהול עומסים (Hassouna, 2005).
ESWT באמת עוזר?
במחקר אקראי אחד הודגם יתרון על פלסבו בהפחתת כאב. התועלת הגבוהה ביותר מתקבלת כחלק מפרוטוקול רב־מרכיבי ולא כטיפול יחיד (Fridman, 2009).
מתי חוזרים לפעילות אחרי ניתוח?
החלמה פונקציונלית מלאה עשויה לארוך שבועות עד חודשים, בהתאם לטכניקה ולמענה הכאב. יש להביא בחשבון סיכון לכאב שארי/היפואסתזיה (Pace, 2010).
מסקנות
מורטון נוירומה היא מצב שכיח אך בר־ניהול היטב. הערכה מוקדמת הכוללת אבחנה קלינית קפדנית ותמיכה בהדמיה לפי צורך מאפשרת להתחיל טיפול שמרני מובנה. הטיפול השמרני כולל שינוי הנעלה, תמיכות מטרטרסליות, ניהול עומסים, טיפול כירופרקטי/פיזיותרפי וטיפולים משלימים. כאשר הכאב עיקש לשקול הזרקות. ניתוח נשקל רק לאחר מיצוי הטיפול השמרני ובהפרעה תפקודית משמעותית. הלקח המרכזי: מי שמטפל מוקדם מקטין סיכוי לכרוניות ולניתוח, ומחזיר את כף־הרגל למסלול של הליכה רכה, ארוכה וללא “אבנים בנעל” (Hassouna, 2005; Fridman, 2009; Pace, 2010).
References:
Fuhrmann, R. A., Roth, A., & Venbrocks, R. A. (2005). Metatarsalgia: Differential diagnosis and therapeutic algorithm. Der Orthopäde, 34(8), 767-775, 769-772, 774-775. (German)
Hassouna, H., & Singh, D. (2005). Morton’s metatarsalgia: Pathogenesis, etiology, and current management. Acta Orthopaedica Belgica, 71(6), 646-655.
Rattray, F., & Ludwig, L. (2000). Clinical Massage Therapy: Understanding, Assessing and Treating Over 70 Conditions. Elmira, ON: Talus Incorporated.
Symeonidis, P. D., Iselin, L. D., Simmons, N., Fowler, S., Dracopoulos, G., & Stavrou, P. (2012). Prevalence of interdigital nerve enlargements in an asymptomatic population. Foot & Ankle International, 33(7), 543-547.
Wu, K. K. (1996). Morton’s interdigital neuroma: A clinical review of its etiology, treatment, and results. Journal of Foot and Ankle Surgery, 35(2), 112-119.
Zipfel, B., & Berger, L. R. (2007). Shod versus unshod: The emergence of forefoot pathology in modern humans. The Foot, 17(4), 205-213.
Pace, A., Scammell, B., & Dhar, S. (2010). The outcome of Morton’s neurectomy in the treatment of metatarsalgia. International Orthopedics, 34(4), 511-515.


