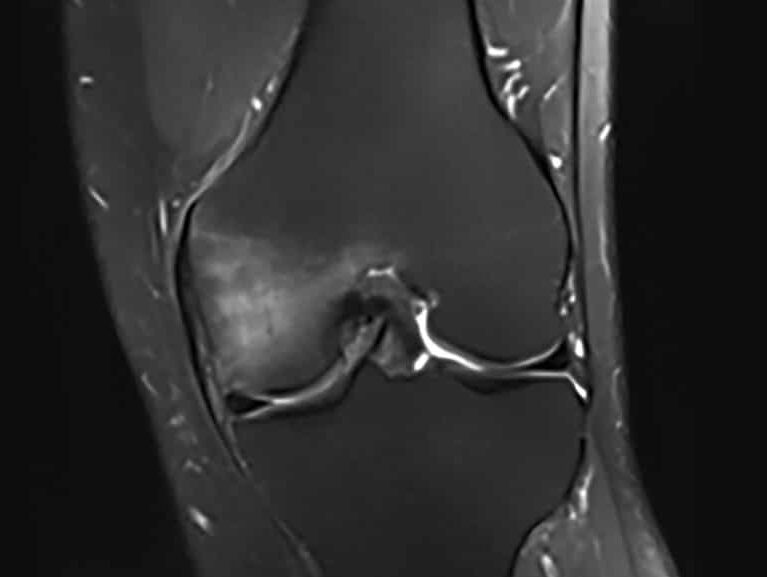
נמק העצם מה גורם לזה? תא עצם שאינו מקבל אספקת דם מת. פגיעה באספקת הדם לירך תגרום: "נמק ראש עצם הירך" (ONFH – Osteonecrosis of the femoral head). שיבוש באספקת הדם לברך יגרום: "נמק ספונטני של הברך" (SONK- Spontaneous Osteonecrosis of the Knee). כאשר הנמק (נמק אווסקולרי) מתרחש במפרק יש סיכון שהעצם מתחת לסחוס לא תעמוד בעומסים ותקרוס. קריסת העצם מתחת לסחוס מחייבת הליך כירורגי מורכב של החלפת המפרק.
סימפטומים של נמק העצם בירך או בברך יכללו כאבים ומגבלות תנועה ברמת חומרה מותאמת לנזק. כאב ברגל היא תלונה שכיחה. ברוב המקרים הגורם לכך הוא נזק זניח כמו מתיחה שריר קלה והכאבים צפויים לחלוף במהרה. לפעמים הגורם לכאבים במפרק עלול להיות נמק אווסקולרי (Avascular necrosis – AVN). אבחון לקוי ו/או ניהול וטיפול לקויים או איטיים עלולים לגרום להרס המפרק. בארצות הברית כ – 10% מכלל הניתוחים להחלפת מפרק ירך מתבצעים בגלל נמק העצם. סימנים ותסמינים אופייניים להפרעה זאת עוזרים במלאכת האבחון.
נמק העצם מה גורם לזה – רקע
כ- 500 מקרים של נמק העצם (Osteonecrosis or Avascular necrosis – AVN) מתרחשים בישראל כל שנה. הסיכוי של נשים ללקות בהפרעה הזאת גבוה משל גברים ביחס של 3:1. לרוב הפרעה זאת מתפתחת בין גיל 30 – 60. נמק בעצם יכול להתפתח בכל אחד מהמפרקים. המפרקים המעורבים בבעיה זאת הם לרוב מפרקים נושאי משקל והנתונים לעומס כגון:
- ירך
- ברך
- כתף
מפרקים אפשריים נוספים כוללים את:
- מפרק הקרסול
- עצמות כף הרגל (Talus fracture)
- עצמות כף היד ומפרק כף היד
- מפרק הלסת
- עמוד השדרה
נמק העצם פוגע בעיקר בקצוות של העצמות בגפיים התחתונות (האפיפיזות) אבל גם בעצמות אחרות. ההשלכות התפקודיות של נמק אווסקולרי תלויות במיקום הנזק ובחומרת הנזק. כאשר הפגיעה קלה יש סיכוי סביר שהעצם שניזוקה תוכל להשתקם באופן מלא. במקרים קשים המוות וההרס של רקמות המפרק ובכלל זה של הסחוס ושל העצם מחייבים החלפת מפרק כירורגית. אבחון מוקדם עשוי למנוע את הקריסה של ראש הירך או של העצם בברך ואת הצורך בהחלפת המפרק בהליך כירורגי מורכב.
גורמים אפשריים לנמק העצם
לא תמיד יש הסבר חד משמעי לגבי מה גורם להפרעה באספקת הדם לעצם. הגורם בחלק גדול מהמקרים נותר עלום. נהוג לחלק את הגורמים להתפתחות נמק בעצם לשתי קבוצות: גורמים טראומטיים וגורמי סיכון שאינם טראומטיים.
גורמים טראומטיים לנמק העצם
נזקי חבלה במפרק מהווים גורם ברור להתפתחות נמק בעצם. נזק טראומטי למפרק יכול להיגרם בשל נפילה, תאונה, פציעת ספורט או ניתוח של המפרק אבל גם מעומסים חוזרניים. הנזקים יכולים להיות:
- סוגים שונים של שבר כולל שבר אי ספיקה
- פריקת מפרק
- נזקים חמורים ברקמות המפרק (קרע מיניסקוס)
הפגיעות הללו עלולות להוביל לפגיעה באספקת הדם והתפתחות נמק העצם ומוות של תאי עצם.
גורמי סיכון שאינם טראומטיים
ישנם גורמי סיכון שאינם טראומטיים לנמק העצם. אלה כוללים בעיקר:
- טיפול תרופתי עם סטרואידים כמו פרדניזון (Prednisone). על פי מחקרים שונים קיימת שכיחות גבוהה במיוחד של נמק בעצם בקרב מטופלים באמצעות סטרואידים. טיפול ארוך (מעל חצי שנה) או מינון גבוה של סטרואידים מעלים את הסיכון. לפי אחת הסברות סטרואידים פוגעים בדפנות כלי הדם ובכך גורמים לשינויים באספקת הדם ולנמק העצם. סברה אחרת טוענת שסטרואידים משנים את המבנה המולקולרי של השומנים בדם וגורמת להם לחסום את כלי הדם ולגרום לנמק העצם. טיפול בסטרואידים גורם לכך שחולים מושתלי כליה סובלים מנמק בעצם בשכיחות גבוהה.
- הפרעות בקרישת דם
- נזקים ומחלות של כלי הדם
- צריכת אלכוהול מוגברת
- אנמיה חרמשית
- כימותרפיה ורדיותרפיה
- מחלת האמודאים (Caisson Disease)
- איידס
- מחלות אוטואימוניות
- תרופות מקבוצת ביספוספונטים (Bisphosphonates) דוגמת פוסלן שמטרתן מניעת אובדן עצם ועוד
- מספר מחקרים מצביעים על האפשרות שקיימת גם נטייה גנטית להתפתחות של נמק בעצם.
סימנים ותסמינים
כאבים
הסימנים והתסמינים וחומרתם תלויים בחומרת הנזק במפרק. בשלב הראשוני במצב של נזק קל בלבד יתכן שלא יהיו סימנים ותסמינים כלל וכלל. במצב מתקדם מעט יותר התסמין העיקרי יהיה:
- כאב קל במפרק המעורב. כך למשל במצב של נמק בעצם הירך הסימנים והתסמינים יכללו כאבים קלים בירך, במפשעה ואולי גם בעכוז
- תחושה של מפשעה תפוסה
- בשלב מתקדם יותר של המחלה הכאבים נעשים קבועים ואינם חולפים עם מנוחה. הכאבים חמורים יותר במהלך השינה בלילה ובכול פעם שאתם מסתובבים במיטה הם מעירים משינה.
- במצב החמור של המחלה הכאבים נעשים חריפים ביותר ובמיוחד כאשר נוצר עומס על המפרק החולה כמו בזמן הליכה או אפילו עמידה. הכאבים הללו צפויים להימשך ללא הפוגה גם במצב של מנוחה. אם נוצר הרס של המפרק הכאבים נעשים קשים עוד יותר.
מגבלות תנועה ותפקוד
גם בכל הנוגע למגבלות תנועה ותפקוד ישנה התפתחות הדרגתית לפי חומרת הנזק:
- כבר בשלב הראשון כאשר הכאב מוגדר כקל החולה יכול להתלונן גם על מגבלות תנועה ומגבלות תפקוד חלקיות. בשלב הזה הכאב במפרק ומגבלות התנועה והתפקוד יהיו קלים יחסית ומנוחה עשויה להקל על הכאב.
- במצב מתקדם יותר של המחלה החולה התלונן על כאבים משמעותיים במצב של מנוחה. הכאבים מחמירים במיוחד כאשר יש עומס על המפרק המעורב. כדי למנוע עומס מיותר וכאבים החולה יתחיל להגביל את המצבים שבהם הוא נושא את משקל גופו כמו בעת הליכה או עמידה.
- בשלב מתקדם עוד יותר הכאבים נעשים קשים וקבועים ומגבלות התפקוד והתנועה מקצינים גם הם.
- במצב החמור ביותר של המחלה ואם מתפתח הרס של רקמות המפרק הכאבים נעשים קשים ביותר. מגבלות התנועה והתפקוד קיצוניים.
הרס של המפרק
אם משטח ההחלקה של המפרק שנחלש מהמחלה נהרס חלקית:
- הכאבים והמגבלות של תנועת המפרק נעשים חמורים במיוחד
- השינוי המבני של המפרק משבש את התפקוד של המפרק
- בטווח הארוך מתפתחת דלקת מפרקים ניוונית על כל המשתמע מכך מבחינת סימנים, תסמינים ותפקוד
כאשר משטח המפרק קורס לחלוטין הסימנים והתסמינים עלולים להחריף הרבה יותר:
- הכאבים קשים במיוחד
- לא ניתן להזיז את המפרק בלי כאבים קשים
- צורך בהחלפת המפרק
נמק העצם היא תופעה שעלולה להימשך זמן ארוך. לעיתים בין תחילת הנמק ועד למצב של קריסת העצם עלולה לחלוף גם יותר משנה. המפרקים המעורבים ביותר הם:
- מפרק הירך
- ומפרק הברך
ולכן במקרה של כאבים בירך וכאבי ברכיים יש לשלול אפשרות של נמק העצם.
נמק העצם בקרב ילדים
מחלת פרתס (Legg Calve Perthes Disease) מתרחשת בשל פגיעה באספקת הדם למפרק הירך בקרב הילדים. לא ברור למה ילדים מסוימים סובלים מהפרעה נדירה זאת. בין ההשערות שהועלו נכללו נטייה גנטית, הפרעות הורמונליות ועוד.
- כאשר המחלה מתפתחת לפני גיל 6 היכולת לריפוי טובה יותר.
- ככל שטווחי התנועה טובים יותר כך משתפרים סיכויי החלמה
- סיכויי ההחלמה של בנות מהפרעה זאת פחות טובים משל בנים
לצורך אבחון מחלת פרתס נעזר:
- בהיסטוריה רפואית שתכלול צליעה, מגבלות תנועה ותפקוןד
- בדיקה גופנית שתאתר מגבלות תנועה וכאב במפרקי הירך המעורבים
- הדמיה של רנטגן ודימות תהודה מגנטית
ברוב המקרים הטיפול הוא:
- שמרני וכולל הסרת העומס ממפרקי הירך, תרגילים לשיפור טווחי תנועה
- במידת הצורך כירורגי
References:
Karel Pavelka, Osteonecrosis, Best Practice & Research Clinical Rheumatology, Volume 14, Issue 2, 2000, Pages 399-414.
Zhang Y, Wang Y, Chen J, Cheng Q, Zhang B, Hao L, Ma T, Qin S, Song W, Wen P. The Top 100 Cited Articles in Osteonecrosis of the Femoral Head: A Bibliometric Analysis. Biomed Res Int. 2021 Aug 21;2021:1433684.
George, Gary BS; Lane, Joseph M. MD. Osteonecrosis of the Femoral Head. JAAOS: Global Research and Reviews 6(5):e21.00176, May 2022.