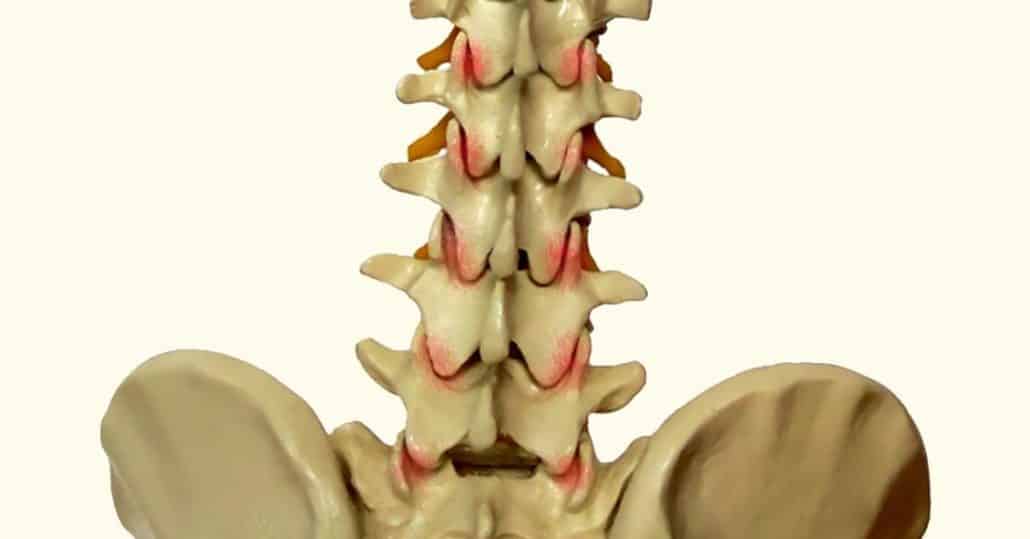
סינדרום פצטלי מותני שכיח הרבה יותר מבלט או פריצת דיסק מותני כגורם לכאב גב תחתון. מפרקי הפצט (Facet joints) או מפרקי השטחה ממוקמים בחלק האחורי של עמוד השדרה. יחד עם הדיסק הבין חולייתי מהווים פרקי השטחה את המפרקים הבין חולייתיים. אופיו הקינטי של עמוד השדרה גורם להשפעות גומלין בין פרקי השטחה לבין הדיסק הבין חולייתי. מסיבה זאת ליקוי באחד יוביל בהכרח לליקוי בשני.
נזקים ושינויים ניווניים במפרקי הפצט נגרמים בגלל עומסי יתר חוזרניים, חבלה ומחלות שונות. דלקת פרקים ניוונית היא המחלה שפגיעתה במפרקים הללו הכי השכיחה. סינדרום פצטלי עלול להתרחש גם בעמוד השדרה הצווארי והגבי. חשוב להגיע לאבחון מדויק של מקור הכאב כדי לטפל בו ביעילות. במאמר "סינדרום פצטלי מותני" נרחיב בנושא.
סינדרום פצטלי מותני – רקע
מפרקי הפצט (Facet joints; מפרקי השטחה/הזיזים) הם מפרקי החלקה סינוביאליים הממוקמים מאחור בכל יחידת תנועה בעמוד השדרה, ויחד עם הדיסק הבין־חולייתי הם מרכיבים את המפרק הבין־חולייתי השלם. מבחינה ביו־מכנית מדובר ב”זוג רצועות היגוי”: הם מגבילים או מאפשרים כיפוף, פשיטה, הטיה וסיבוב בהתאם לזווית המפרק בכל אזור, צוואר, גב עליון, מותני (Cohen, 2007; Neumann, 2017). כל ליקוי בדיסק משנה את חלוקת העומסים על הפצט ולהפך. לכן נזק במרכיב אחד של היחידה הבין־חולייתית נוטה “לגלוש” אל האחר (Cohen, 2007).
הערכת שכיחות מבוססת חסימות אבחנתיות מצביעה על כך ש- 15-45% מהסובלים מכאב גב תחתון כרוני (LBP) מקורם הוא סינדרום פצטלי מותני. שיעור זה הוא לרוב גבוה מזה של כאב דיסקוגני או רדיקולרי באוכלוסיות מרפאה כלליות (Schwarzer, 1994; DePalma, 2011; Cohen, 2007). ועדיין, במרפאות רבות סינדרום פצטלי מותני נותר תת־מאובחן, משום שהיסטוריה ובדיקה גופנית לבדן אינן ספציפיות דיה (Cohen, 2007; Boubagra, 2018).
מה קורה שם? פתופיזיולוגיה בשלושה צירים
ניוּון/עומס חוזר
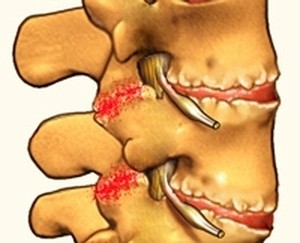
שחיקת הסחוס, היפרטרופיה של קפסולה ואוסטאופיטים עקב עומסים חוזרניים, ישיבה ממושכת, היפר־לורדוזיס או חבלות (Cohen, 2007; Boubagra, 2018).
דלקת סינוביאלית/קפסולרית
ריבוי סיבי עצב תחושתיים בקפסולה מפיק כאב מקומי חד־משמעי ואף כאב מושלך (Cohen, 2007).
שינויי יציבה/שרשרת קינמטית
ירידה בתנועתיות סגמנטלית והפעלת יתר של זוקפי גב גורמות לספאזם משני, שמחמיר מגבלות וכאב (Neumann, 2017).
גורמים וגורמי סיכון
גורמים אפשריים להתפתחות סינדרום פצטלי מותני כוללים:
- עומסי יתר חוזרניים: פעולות, מטלות ומנחים הגורמים לעומס יתר או עומס חוזרני על חוליות עמוד השדרה מעלים את הסיכון לנזקים מצטברים בין היתר גם למפרקים הפצטלים ולרקמות הסובבות אותם.
- גיל: דגנרציה מצטברת של הסחוס והקפסולה (Boubagra, 2018).
- עודף משקל/השמנה: עומס מכני גבוה ותבניות תנועה פחות יעילות (Thijssen, 2015).
- ישיבה ממושכת/יציבה לקויה: העמסת יתר סטטית על יחידות תנועה מותניות (Kett, 2021).
- ליקויים ציריים/מבניים: עקמת, היפר־/היפו־לורדוזיס (Neumann, 2017).
- פציעות מוקדמות/דיסקוגניות: בלט/קרע טבעתי שמשנים חלוקת עומסי גזירה ודחיסה (Cohen, 2007).
סימנים ותסמינים
הסימנים והתסמינים העיקריים בגין סינדרום פצטלי מותני כוללים כאב מקומי בעיקרו, בגב התחתון, עם הקרנה קצרה לישבן/ירך אחורית (אך ללא סימנים נוירולוגיים מכווני־שורש). מאפיינים שכיחים:
- מוחמר בפשיטה (הקשתה לאחור), בהליכה איטית/עמידה סטטית (“הליכת מוזיאון”), בשטיפת כלים, בעמידה בתור.
- מוקל בכפיפה (ישיבה, תנוחה עוברית, רכיבה על אופניים), ובהליכה נמרצת יותר (Cohen, 2007).
- נוקשות בוקר/אחרי מנוחה שמתרככת עם תנועה עדינה; לעיתים ספאזם זוקפי גב מגן (Neumann, 2017).
- מבחנים פרובוקטיביים כמו Kemp’s (כיפוף־צד + פשיטה) או כאב בלחיצה סגמנטלית אחורית (springing) עשויים לשחזר כאב אך אינם ספציפיים (Cohen, 2007).
למה קשה לאבחן סינדרום פצטלי מותני?
היסטוריה ובדיקה גופנית מועילות לסבירות מקדימה, אך אינן “חותמות” אבחנה של סינדרום פצטלי מותני. הדמיה (צילום/CT/MRI) מדגימה שינויים ניווניים שכיחים גם בא־סימפטומטיים, וקורלציה בינם לבין סימפטומים מוגבלת (Boubagra, 2018). לכן, כאשר נדרשת ודאות גבוהה, למשל לפני התערבות פולשנית, מקובל להשתמש בחסימות עצביות או הזרקה תוך־מפרקית מקומית לאבחון. הקלה זמנית ומשמעותית בכאב לאחר ההזרקה תומכת באבחון של סינדרום פצטלי מותני (Cohen, 2007; Boubagra, 2018). גם לשיטה זו יש שיעור חיובי־שגוי לא מבוטל. לכן מקובל לבצע לעיתים שתי חסימות עם חומרי הרדמה בעלי משך שונה ולדרוש תגובה עקבית (Cohen, 2007).
דגלים אדומים
הסימנים והתסמינים הבאים מהווים דגלים אדומים המחייבים בירור רפואי דחוף:
- חום, ירידה במשקל לא מוסברת, טראומה משמעותית, חסר נוירולוגי פרוגרסיבי/הפרעות סוגרים (Qaseem, 2017).
אבחנה מבדלת של סינדרום פצטלי מותני
- דיסקוגני/רדיקולרי: כאב מקרין מתחת לברך, סימן לסג, חסר תחושתי/כוח (Cohen, 2007).
- היצרות תעלת השדרה: החמרה בהליכה, הקלה בכפיפה; לעיתים נימול/חולשה.
- כאב שמקורו סקרואילאיטיס: כאב אגפי/ישבני עם מבחני עומס סקרו־איליאק חיוביים.
- כאב ממקור פנימי: כליה/אאורטה/לבלב לפי קליניקה.
- שלבקת חוגרת : פריחה עורית.
טיפול: תחילה שמרני, ובהמשך ממוקד
ההנחיות המודרניות לכאב גב כרוני מדגישות התערבויות לא תרופתיות כקו ראשון, הכוללות פעילות גופנית, חינוך, טיפול ידני/מנואלי לפי צורך. טיפול רב־מערכתי הכולל משככי כאב/NSAIDs הניתנים בזהירות ולטווח קצר (Qaseem, 2017; Hayden, 2021).
1) חינוך, ארגונומיה וניהול עומסים
- הפחתת עמידה סטטית ו“הליכת מוזיאון”, חלוקת משימות, החלפת עמידה בישיבה דינמית/הליכה נמרצת קצרה.
- שינה: הימנעות משכיבה על הבטן; עדיפות לשכיבה צדית עם כרית בין הברכיים או על הגב עם תמיכה מתחת לברכיים להפחתת פשיטה מותנית.
- ארגונומיה: מסך בגובה עיניים, תמיכה לומברית, החלפות תנוחה תכופות (Kett, 2021).
2) תרגול ממוקד ותיקון דפוסים
העדויות לכאב גב כרוני תומכות במגוון תכניות פעילות כולל חיזוק/סבולת, יציבה, יוגה, פילאטיס., התנסות מדורגת כוללת יתרון מתון עד בינוני בכאב/תפקוד (Hayden, 2021). בפצטלי מותני נתמקד ב־
- שליטה לומבו־אגנית: מייצבי ליבה, שרירי עכוז, זוקפי גב במינונים נמוכים־בינוניים (Neumann, 2017; Hayden, 2021).
- ניידות קפסולרית עדינה: מוביליזציות כיפוף/הטיה; מתיחות מכופפי ירך וחזה לתיקון היפר־לורדוזיס.
- הדרגתיות בעומסים אחוריים: חזרה מדודה לפשיטה לפי סף כאב.
3) טיפול ידני/מנואלי
מוביליזציה/מניפולציה של עמוד השדרה עשויות לספק הקלה קצרת־טווח כחלק מתכנית רב־מערכתית. השפיעה זאת מתגברת כאשר הטכניקות הללו משולבות בתרגול אקטיבי (Rubinstein, 2019; Qaseem, 2017). המטרה איננה “ליישר חוליות”, אלא לשפר תנועתיות סגמנטלית, להפחית רגישות ולפתוח “חלון אימון”.
4) תרופות
NSAIDs או משככי כאב לתת לטווח קצר ובהתאם לפרופיל סיכון. ההשפעה היא זמנית ואין עדות לתועלת ארוכת טווח. אופיואידים אינם מומלצים לכאב גב כרוני שאינו ממאיר (Qaseem, 2017).
5) התערבויות בהדמיה (אם שמרני מיטבי לא הספיק)
- הזרקות תוך־מפרקיות/ענף מדיאלי עם סטרואיד: עשויות להקל זמנית בחלק מן המטופלים, אך התועלת ארוכת־טווח מוגבלת. ערכן בעיקר אבחנתי/חלון שיקום (Cohen, 2007; Boubagra, 2018).
- אבלציה בגלי רדיו (RFA) של הענף המדיאלי: לאחר חסימות אבחנתיות חיוביות, יכולה לספק הקלה למשך חודשים ואף עד שנה בחלק מהמטופלים (Manchikanti, 2020; Cohen, 2007). בחירה נכונה (אבחון קפדני, טכניקה מונחית הדמיה) קריטית להצלחה.
- ניתוח: נדיר ונשקל רק בהקשר עיוותים/אי־יציבות/פתולוגיות נלוות. סינדרום פצטלי מבודד אינו אינדיקציה ניתוחית שכיחה (Cohen, 2007).
סינדרום פצטלי מותני – טיפול כירופרקטי
טיפול כירופרקטי בהתפתחות סינדרום פצטלי מותני מתמקד:
- בהפחתת עומסי־שיא על מפרקי הפצט.
- שיפור תנועתיות סגמנטלית.
- חיזוק שרירי ליבה
- החזרת שליטה לומבו־אגנית.
בליבת הגישה:
- אבחון ביו־מכני ממוקד (זיהוי פשיטה מכאיבה, “הליכת מוזיאון”, ספאזם זוקפי גב).
- התאמות ארגונומיות ושינויי הרגלים (הפחתת עמידה סטטית, תנוחות שינה מקלות).
- טיפול מנואלי מדוד הכולל מוביליזציה/מניפולציה שפותח “חלון” ליישום תרגול אקטיבי.
- סקירת Cochrane עדכנית מצאה שלטיפול מנואלי בעמוד שדרה יש השפעה מיטיבה בכאב ותפקוד בכאב גב תחתון כרוני כאשר הוא משתלב בתכנית פעילה. התועלת גדלה כשמוסיפים חינוך ותרגול (Rubinstein, 2011).
- הנחיות הקולג׳ האמריקאי לרופאים ממליצות להתחיל בכאב גב כרוני בהתערבויות לא תרופתיות, ובהן טיפול מנואלי, תנועה מודרכת ופעילות גופנית, לפני תרופות או פולשנות. זה מתיישב היטב עם הפרוטוקול הכירופרקטי השמרני (Qaseem, 2017).
תכנית פעולה בת 8-12 שבועות: דוגמה פרקטית
שבוע 1-2
- חינוך: “הפחת סטטיקה, הוסף תנועה קצרה תכופה”.
- ארגונומיה בבית/עבודה; הנחיות שינה.
- תרגול יומי 10-12 דק׳: נשימה/הארכת בית חזה, כפיפה עדינה בשכיבה, מתיחות מכופפי ירך, כריעה חלקית נתמכת.
- כאב אקוטי: NSAID קצר־טווח לפי צורך/הנחיה; הימנעות ממנוחה במיטה.
שבוע 3-6
- חיזוק מייצבים: גשרונים, dead bug, bird-dog, חיזוק שרירי עכוז (קונטרה־לטרלי).
- ניידות: מוביליזציות כיפוף/הטיה; הוספת פשיטה קלה ללא כאב (10-20% טווח).
- הליכה נמרצת 20-30 דק׳, 4-5×שבוע.
- טיפול ידני אחת לשבועיים לפתיחת תנועה ושחרור ספאזם.
שבוע 7-12
- פרוגרסיה עומס־זמן לפני עומס־עוצמה; הוספת תרגילים פונקציונליים (הושטת יד בעמידה, hip hinge) עם ניטרל לומברי.
- הערכת תפקוד: ירידה בנוקשות בוקר, שיפור זמן עמידה/הליכה לפני כאב, ירידה בתרופות.
- אם למרות היענות גבוהה נשאר כאב מגביל – דיון בהזרקה אבחנתית/טיפולית ובהמשך RFA לפי התאמה.
- כללי “תמרור כאב”: כאב ≤3/10 מותר, 4-5/10 הורד מינון/טווח, ≥6/10 עצור ושנה.
שאלות נפוצות ותשובות קצרות
האם MRI “יראה” פצע פצטלי?
יכול להדגים שינויים ניווניים/בצקת פריארטיקולרית, אך הקורלציה לתסמינים מוגבלת. חסימות אבחנתיות מדויקות יותר לקביעת מקור הכאב (Boubagra, 2018; Cohen, 2007).
האם הליכה מזיקה לפצט?
הליכה נמרצת לרוב מועילה. תנועה דינמית ללא פשיטה ממושכת מקלה על הכאב. עמידה סטטית/הליכה איטית ממושכת מחמירות (Cohen, 2007).
מה הסיכוי שהכאב “יעבור לבד”?
בחלק גדול מהמקרים של סינדרום פצטלי מותני ועם ניהול עומסים ותרגול התשובה היא כן. במקרים עקשניים, הזרקות/RFA נשקלות לאחר אבחון קפדני (Qaseem, 2017; Manchikanti, 2020).
השורה התחתונה
סינדרום פצטלי מותני הוא גורם שכיח לכאב גב תחתון כרוני לעיתים קרובות יותר מאשר בלט/פריצת דיסק אך אינו תמיד מזוהה בזמן. אבחנה טובה נשענת על קליניקה, שלילת דגלים אדומים, והבנה שממצאי הדמיה לבדם אינם מספיקים; כשנדרשת ודאות, חסימות אבחנתיות הן הזהב. הטיפול מתחיל בשיקום שמרני רב־מערכתי הכולל חינוך, ארגונומיה, תרגול ו/או טיפול ידני ולאחר מיצויו, בהתערבויות ממוקדות (הזרקות, RFA) לפי קריטריונים ברורים. עם בחירה נכונה ופרוטוקול הדרגתי, רוב המטופלים חוזרים לפעילות מלאה עם פחות כאב ויותר שליטה (Cohen, 2007; Hayden, 2021; Manchikanti, 2020).
סינדרום פצטלי מותני – מניעה
מניעה ושימור, מה באמת עושה הבדל:
- תנועה תדירה: מיקרו־הפסקות של 1-2 דק׳ כל 30 דק׳ בעמידה/ישיבה.
- כוח־סבולת ליבה/גלוטאוס פעמיים־שלוש בשבוע.
- ניהול משקל: מפחית עומס מכני ודלקת מערכתית (Thijssen, 2015).
- היגיינת שינה: מנחים מקלים, מזרן/כרית תומכים.
- בריאות נפשית: הפחתת סטרס משפרת טונוס שריר ועמידות לכאב (Qaseem, 2017).
מכתב תודה על טיפול בכאב גב מותני.
References:
Boubagra, K., Grand, S., & Krainik, A. (2018). Facet joint syndrome: From diagnosis to interventional management. Insights into Imaging, 9(6), 773-789.
Cohen, S. P., & Raja, S. N. (2007). Pathogenesis, diagnosis, and treatment of lumbar zygapophysial (facet) joint pain. Anesthesiology, 106(3), 591-614.
DePalma, M. J., Ketchum, J. M., & Saullo, T. R. (2011). What is the source of chronic low back pain and does age play a role? Pain Medicine, 12(2), 224-233.
Hayden, J. A., Ellis, J., Ogilvie, R., Malmivaara, A., & van Tulder, M. W. (2021). Exercise therapy for chronic low back pain: An updated systematic review and meta-analysis. Cochrane Database of Systematic Reviews, 2021(9), CD009790.
Kett, A. R., Sichting, F., & Milani, T. L. (2021). The effect of sitting posture and postural activity on low back muscle stiffness. Biomechanics, 1, 214-224.
Manchikanti, L., Kaye, A. D., Soin, A., et al. (2020). Responsible, safe, and effective use of facet joint interventions in managing chronic spinal pain: American Society of Interventional Pain Physicians (ASIPP) guidelines. Pain Physician, 23(3S), S1-S127.
Neumann, D. A. (2017). Kinesiology of the musculoskeletal system: Foundations for rehabilitation (3rd ed.). Elsevier.
Qaseem, A., Wilt, T. J., McLean, R. M., & Forciea, M. A. (2017). Noninvasive treatments for acute, subacute, and chronic low back pain: A clinical practice guideline from the American College of Physicians. Annals of Internal Medicine, 166(7), 514-530.
Rubinstein, S. M., Terwee, C. B., Assendelft, W. J. J., et al. (2019). Spinal manipulative therapy for chronic low-back pain: An updated systematic review and meta-analysis. Cochrane Database of Systematic Reviews, 2019(9), CD008112.
Schwarzer, A. C., Wang, S. C., O’Driscoll, D., Harrington, T., & Bogduk, N. (1994). The ability of clinical features to predict lumbar zygapophysial joint pain. Spine, 19(10), 1132-1137.
Thijssen, E., van Caam, A., & van der Kraan, P. M. (2015). Obesity and osteoarthritis: More than just wear and tear – Pivotal roles for inflamed adipose tissue and dyslipidaemia. Rheumatology (Oxford), 54(4), 588-600.