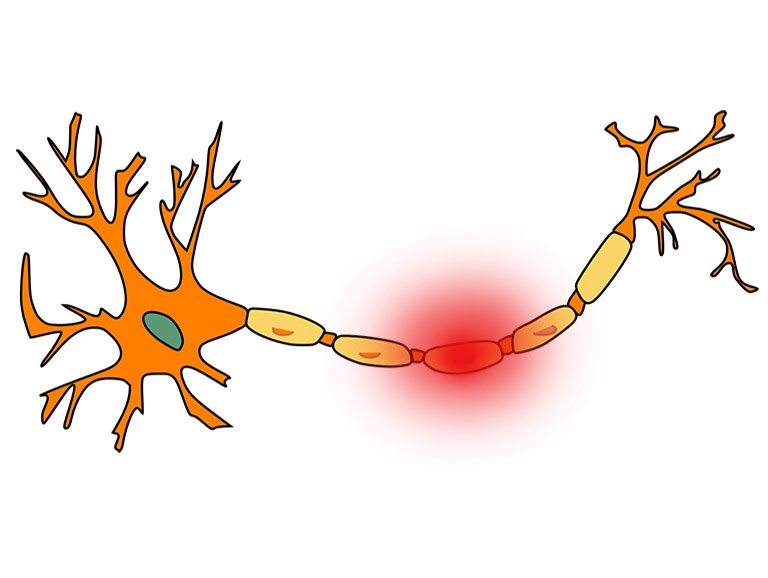
כאב בגלל נזק עצבי היא תופעה שכיחה. לא תמיד קל לזהות שהכאב נובע מנזק עצבי ולא מפציעת רקמה אחרת במערכת שריר ושלד. כאבים במערכת שריר ושלד יופיעו כאשר אחת או יותר מהרקמות המרכיבות את המערכת הזאת נפגעות. בין הרקמות המרכיבות את מערכת שריר ושלד נמנה שרירים, גידים, סיבי עצב, סחוסים, מפרקים ועוד.
הרבה פעמים נזק עצבי (neuropathy) יוביל להתפתחות סימנים ותסמינים נוספים מלבד כאב. שיבוש העברת האותות החשמליים הנגרם בגלל נזק עצבי עלול להוביל להתפתחות סימנים ותסמינים נוספים. בין הסימפטומים האופייניים לפגיעה עצבית נמנה בין היתר נימול, חולשה, סחרחורת, ליקויים קוגניטיביים ועוד. סימנים ותסמינים אלו עשויים לעזור לנו לזהות את העצב שניזוק ולעריך את חומרת הנזק. במאמר הבא "כאב בגלל נזק עצבי" נדון בנושא הזה בהרחבה.
כאב בגלל נזק עצבי – רקע אנטומי
הגוף שלנו נשלט ומבוקר באמצעות מערכת העצבים. מקובל לחלק את מערכת העצבים לשתים: מערכת העצבים המרכזית (central nervous system) ומערכת העצבים הפריפרית (autonomic nervous system). מערכת העצבים הפריפרית כוללת בתוכה גם את מערכת העצבים האוטונומית.
- מערכת העצבים המרכזית: המוח, המוח הקטן וחוט השדרה מרכיבים את מערכת העצבים המרכזית. תפקידיה של המערכת הזאת כוללים קליטת מידע מחלקי הגוף השונים, עיבודו והוצאת הנחיות לביצוע.
- מערכת העצבים הפריפרית: סיבי העצב הבוקעים מחוט השדרה ומעצבבים את חלקי הגוף השונים יוצרים את מערכת העצבים הפריפרית. תפקידיה של מערכת העצבים הפריפרית כוללים העברת מידע תחושתי ומוטורי מחלקי הגוף השונים אל המוח. מערכת העצבים האוטונומית מתייחסת לשתי מערכות משלימות:
- מערכת העצבים הסימפתטית הפועלת במצבי חירום וסכנה בין היתר באמצעות תגובת הילחם או ברח. בין הפעולות של מערכת זאת נמנה האצת קצב הלב, הגברת לחץ הדם וקצב הנשימה ועוד.
- מערכת העצבים הפאראסימפתטית פועלת לתחזוקת הגוף במצבי שגרה באמצעות ויסות ובקרה של איברים פנימיים. בין הפעולות של מערכת זאת נמנה האטת קצב הלב, הרחבת כלי הדם, שיפור מערכת העיכול ועוד.
במאמר "כאב בגלל נזק עצבי" נפרט בין היתר מהו כאב עצבי.
מהו כאב עצבי
כאב נוירופתי הוא כאב שנובע מפגיעה או ממחלה של מערכת העצבים הסומטוסנסורית – ההולכה התחושתית והמוטורית שמקשרת בין מוח, חוט שדרה ועצבים פריפריים (Finnerup, Kuner, & Jensen, 2021). להבדיל מכאב נוּציספטיבי “רגיל” שמקורו בפגיעה ברקמות (שריר, גיד, סחוס, עור), כאב נוירופתי מתאפיין לעיתים בתחושות שריפה, דקירות, חשמל, נימול ועקצוץ, ובהעצמה לא-פרופורציונלית של כאב לגירויים קלים (אלודיניה) או רגישות־יתר לכאב (היפראלגזיה) (Colloca et al., 2017).
ההגדרה הרחבה של כאב כ“חווייה תחושתית ורגשית בלתי נעימה הקשורה, או דומה לזו הקשורה, לנזק ממשי או אפשרי לרקמות” מזכירה לנו שהכאב אינו רק אות פיזי טהור אלא גם חוויה מוחית־רגשית (Raja et al., 2020). משום כך, כאב נוירופתי כרוני משפיע עמוקות על שינה, מצב רוח, תפקוד יומיומי ואיכות חיים, ולעיתים אינו מגיב למשככי כאבים מקובלים ודורש גישה רב־תחומית המתאימה מנגנון לטיפול (Finnerup et al., 2015).
מה השכיחות של כאב עצבי?
כאב עם מאפיינים נוירופתיים נפוץ יותר מכפי שנדמה. סקירה סיסטמטית רחבה העריכה ששכיחות כאב בעל מאפיינים נוירופתיים באוכלוסייה הכללית נעה סביב 6.9%-10% (van Hecke, Torrance, & Smith, 2014). מחקרי אוכלוסייה עדכניים אף מצאו שיעור כולל של כ-9% באוכלוסייה בוגרת, עם שכיחות גבוהה יותר בקבוצות סיכון. לדוגמה, בקרב אנשים עם סוכרת, לאחר כימותרפיה, או לאחר ניתוחים/פציעות עצביות (Baskozos et al., 2023).
מעבר להופעה, ההשפעה קלינית־חברתית משמעותית: כאב נוירופתי כרוני נקשר יותר לדיכאון, בידוד, ירידה בתפקוד וצריכת שירותי בריאות מוגברת בהשוואה לכאב לא-נוירופתי (Murnion, 2018). לנוכח הזדקנות האוכלוסייה, שיעור הסוכרת הגואה ושיעורי הישרדות גבוהים יותר לאחר טיפולים אונקולוגיים, צפוי שהנטל יתמיד ואף יעלה (Colloca et al., 2017).
גורמים אפשריים לכאב עצבי
מקובל לחלק את מערכת העצבים לשתי תת-מערכות עיקריות: מערכת העצבים המרכזית (CNS – מוח, מוחון, חוט שדרה) ומערכת העצבים הפריפרית (PNS – שורשי עצבים ועצבים היקפיים); האחרונה כוללת גם את המערכת האוטונומית (Raja et al., 2020). פגיעה בכל אחד ממרכיבי הציר הזה יכולה להוביל לכאב נוירופתי. פגיעה במערכת העצבים המרכזית (למשל, לאחר שבץ) או פגיעה במערכת העצבים הפריפרית (למשל, נוירופתיה סוכרתית).
דוגמאות שכיחות
להלן מספר דוגמאות של הפרעות בריאותיות הגורמות הגורמות לכאב עצבי:
- נוירופתיה פריפרית סוכרתית: פגיעה הדרגתית בסיבי עצב תחושתיים-אוטונומיים, לרוב בכפות הרגליים, עם שריפה, נימול וחולשה (Finnerup et al., 2021).
- פוסט-הרפטית (שלבקת חוגרת): כאב צורב/דוקר באזור דרמטומי אחרי זוסטר.
- רדיקולופתיה (לדוגמה צווארית/מותנית): לחץ/דלקת על שורש עצב, לעיתים מכאב מוקרן לאורך גפה (Finnerup et al., 2015).
- נוירלגיה טריגמינלית: התקפי “חשמל” חדים בפנים.
- כאב מרכזי לאחר שבץ: פגיעה במסלולים תחושתיים מרכזיים.
- נוירופתיות לכידה: תסמונת התעלה הקרפלית/קוביטלית, פרונאלית, טיביאלית ועוד.
- כאב עצבי נוירופתי לאחר טיפול רפואי: לדוגמה, פגיעת עצב לאחר ניתוח או כימותרפיה (Colloca et al., 2017).
גורמים מתווכים ומחמירים
להלן מספר גורמי סיכון המגבירים את הסיכון לפגיעה עצבית ולכאב נוירופתי (Cavalli et al., 2019):
- אי-איזון גליקמי.
- חסרים ויטמינריים (B12).
- עישון.
- חשיפה לטוקסינים (כולל חלק מתרופות).
- מחלות אוטואימוניות ומטבוליות.
מנגנונית, מדובר בשילוב של פעילות אקטופית באקסונים פגועים, סנסיטיזציה פריפרית ומרכזית, שינויים דלקתיים ופלסטיות במעגלי כאב (Finnerup et al., 2021).
סימפטומים אפשריים
כאב עצבי (נוירופתי) מתאפיין במגוון עושר של תסמינים:
- כאבים ספונטניים: שריפה/דקירה/”חשמל”, לעיתים עם תנודות מעת לעת.
- כאב מושרה: אלודיניה (כאב ממגע קל) והיפראלגזיה (תגובת-יתר לגירוי כואב).
- סימפטומים תחושתיים־שליליים: ירידה בתחושה, “רדימות”, נימול, אובדן פרופריוספציה.
- סימנים מוטוריים/אוטונומיים: חולשה, עוויתות שריר, הזעה/שינויים וסקולריים מקומיים.
- לוויינים מערכתיים: הפרעות שינה, עצבנות/דיכאון, עייפות, ירידה בתפקוד (Attal, Bouhassira, & Baron, 2018).
- בפגיעה CNS (למשל, לאחר שבץ או פגיעה מוחית) עשויות להופיע גם הפרעות קואורדינציה, שיווי משקל, דיבור או קוגניציה.
- בפגיעה מוחונית: אטקסיה, דיסמטריה, ורטיגו.
- ובפגיעה בחוט השדרה – סימנים “פירמידליים”, שינויי רפלקסים והפרעות סוגרים, כשכלל התסמינים מופיעים מתחת לגובה הפגיעה (Colloca et al., 2017).
עצבים פריפריים המרבים להינזק
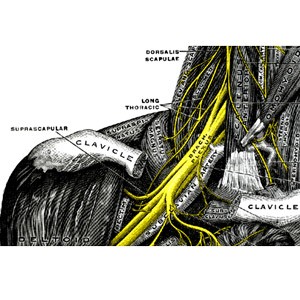 עצבים פריפריים הנמצאים בסיכון גבוה במיוחד להינזק כוללים בין היתר את העצבים הבאים:
עצבים פריפריים הנמצאים בסיכון גבוה במיוחד להינזק כוללים בין היתר את העצבים הבאים:
- העצב הסיאטי (סכיאטיקה).
- העצב הפרוניאלי המשותף (צניחת כף רגל).
- שורש עצב צווארי.
- עצב החישור במרפק.
- עצב הגומד (תסמונת התעלה הקוביטלית).
- עצב התווך (תסמונת התעלה הקרפלית).
- העצב הפמורלי (מרלגיה פרסטטיקה).
- העצב הטיביאלי (תסמונת התעלה הרדיאלית).
- עצב בין אצבעות הרגליים (מורטון נוירומה).
אבחון
האבחון משלב אנמנזה מדוקדקת, בדיקה נוירולוגית, מבחני סינון וכלים עזר. ה”זהב” האבחוני הוא הוכחת פגיעה במערכת הסומטוסנסורית המתאימה לפיזור הכאב, יחד עם מאפיינים נוירופתיים אופייניים (Attal et al., 2018).
אנמנזה
נברר פרטים שיסייעו להעלות חשד לנוירופתיה:
- מיפוי מדויק של האזורים הכואבים/רדומים (דרמטומי/מיוטום)
- זיקה לעומס/טראומה/ניתוח, תרופות, מחלות רקע (סוכרת, מחלות מערכתיות)
- תיאור הכאב (שריפה/חשמל, אלודיניה)
בדיקה
בשלב הזה נבצע:
- הערכת כוח, תחושה (חד/קהה, חום/קור, רטט), רפלקסים
- מבחני לכידה עצבית מקומיים (לדוגמה, תסמונת התעלה הקרפלית)
- תמרוני שורש עצב (לדוגמה, SLR לרדיקולופתיה מותנית) (Finnerup et al., 2015).
כלים משלימים
בין יתר הכלים המשלימים שבהם נוכל להיעזר נציין:
- שאלוני סקר כמו DN4, painDETECT ו-S-LANSS המסייעים בהערכת סבירות לכאב עצבי נוירופתי במרפאה (Attal et al., 2018).
- בדיקות הולכה עצבית/EMG רלוונטיות לנוירופתיות פריפריות.
- MRI/CT יסייעו בהדגמת לחץ שורשי, נגעים מרכזיים או לליקויים אנטומיים.
- בדיקות דם כוללות גלוקוז/המוגלובין מסוכרר, B12, תפקודי בלוטת תריס ומדדי דלקת לפי הצורך (Colloca et al., 2017).
“דגלים אדומים”
חולשה מתקדמת, הפרעות סוגרים חדשות, ירידה תחושתית נרחבת, ירידה חדה במשקל, חום, או סיפור אונקולוגי. קיומם מצדיק בירור מיידי והפניה דחופה (Raja et al., 2020).
טיפול
כאב נוירופתי “לא משחק לפי הכללים” של משככי כאבים נפוצים; בדרך כלל נדרש טיפול ממוקד-מנגנון, רב־תחומי, המשלב תרופות, שיקום, חינוך, וטיפול בגורם הבסיסי (Finnerup et al., 2015).
א. טיפול תרופתי (המלצות קו-ראשון/שני/שלישי)
קונסנזוס עדכני מדגיש תרופות נוירומודולטוריות כקו ראשון:
- נוגדי דיכאון טריציקליים (כגון אמיטריפטילין),
- מעכבי ספיגה חוזרת סרוטונין-נוראדרנלין (SNRIs: דולוקסטין/ונלפקסין),
- גאבאפנטינוּאידים (גאבאפנטין/פרגאבאלין).
- המלצות קו שני: מדבקות לידוקאין, מדבקות קפסאיצין בריכוז גבוה ו-טרמדול.
- המלצות קו שלישי: אופיואידים חזקים או בוטולינום-טוקסין A במצבים סלקטיביים (Finnerup et al., 2015; Soliman et al., 2025).
בבחירת התרופה יש להתחשב בתחלואה נלווית (למשל דיכאון, הפרעות שינה), תופעות הלוואי הפוטנציאליות, אינטראקציות ושיקולי גיל (Murnion, 2018).
ב. טיפול שיקומי-התנהגותי
התערבויות חינוך לכאב (pain education), פעילות גופנית מדורגת, פיזיותרפיה ותרגילי תחושה (desensitization, graded motor imagery) מסייעים בשבירת מעגל הימנעות-כאב ובלשיפור תפקוד (Baskozos et al., 2023). עבור לכידות עצב פריפריות – סדים/קיבוע זמני, שינויי ארגונומיה ותנועתיות עצבית (nerve gliding) יכולים להפחית עומס עצבי (Attal et al., 2018).
ג. נוירומודולציה לא פולשנית וגישות התנהגותיות
במקרים עמידים: TENS, גירוי מגנטי מוחי חוזר (rTMS) או התערבויות CBT ממוקדות כאב עצבי עשויים להפחית עוצמה ולשפר שליטה עצמית (Soliman et al., 2025).
ד. טיפול בגורם הבסיסי
איזון גליקמי בסוכרת, תיקון חסר B12, הפסקת עישון, התאמת/החלפת תרופה פוגעת עצב. כולם צעדים הכרחיים לצד טיפול סימפטומטי (Cavalli et al., 2019).
טיפול כירופרקטי: היכן הוא נכנס?
טיפול כירופרקטי אינו “תרופת-קסם” לכאב עצבי נוירופתי, אך הוא יכול לשמש רכיב משלים יעיל כשמקור הכאב כולל מרכיב מכני-שרירי/שלדי (למשל, רדיקולופתיה קלה, לכידה פריפרית, עומסי-יתר צוואריים/מותניים), וכאשר נדרש תיקון עומסים, יציבה ותנועה (Murnion, 2018; Attal et al., 2018).
מה כולל בדרך כלל הטיפול הכירופרקטי?
- אבחון מכני-תפקודי של עמוד השדרה, חגורת הכתפיים/אגן והגפיים לזיהוי מקורות לחץ/חיכוך על מסלולי עצב.
- טיפול ידני עדין (mobilization/מניפולציות מבוקרות במידת הצורך), שחרור רקמות רכות, וטכניקות המכוונות להורדת מתח סביב גידים/פאסיות המפעילים גירוי עצבי.
- היגיינת עצב: תרגילי nerve glides (למשל, לעצב המדיאני בתעלה הקרפלית), שיפור סבילות עומס הדרגתי ותיקון דפוסי תנועה.
- ארגונומיה: התאמת סביבת עבודה/שינה, שינויי תנוחה, הפסקות תנועה, סדים זמניים (לדוגמה בשורש כף היד).
- תיאום רב-מקצועי: שילוב עם פיזיותרפיה, רופא משפחה/נוירולוג וניהול תרופתי – בהתאם להנחיות המבוססות-ראיות (Finnerup et al., 2015).
חשוב לציין:
הראיות החזקות ביותר להפחתת כאב נוירופתי עדיין מתייחסות בעיקר לטיפול תרופתי/נוירומודולטורי. טיפול כירופרקטי נוטה להיות יעיל במיוחד כאשר קיימת תרומה מכנית (לכידה, עומסים, תפקוד מפרקי לקוי). אינו יעיל כאשר מדובר בכאב מרכזי “טהור” (Colloca et al., 2017). לפיכך, ההתאמה נעשית אינדיבידואלית, תוך מעקב אחר תוצאות ובטיחות.
דוגמאות לפי מיקום
- תסמונת התעלה הקרפלית: כאב/נימול אגודל-אמה; טיפול ראשוני – סד לילה, ארגונומיה, תרגילי החלקת עצב; ניתן לשלב טיפול ידני עדין, ובהיעדר תגובה לשקול הזרקה/ניתוח (Attal et al., 2018).
- רדיקולופתיה מותנית: כאב מקרין לאורך הרגל; התערבות מוקדמת בניהול עומס, תרגילי מקנזי, חיזוק ליבה ו-manual therapy עדינה עשויים להועיל; במקביל ניהול תרופתי/הדמיה לפי צורך (Finnerup et al., 2015).
- נוירופתיה סוכרתית: הדגשה על איזון סוכר, חינוך כף רגל, פעילות מבוקרת ואימוני תחושה; התערבות ידנית מתונה בלבד להקלה שרירית-שלדית נלווית (Murnion, 2018).
סיכום
כאב בגלל נזק עצבי הוא אתגר קליני נפוץ ומורכב, הפוגע קשות באיכות החיים ותפקוד. ההבחנה בין כאב נוירופתי לכאב נוּציספטיבי חשובה – מאחר שמסלולי הכאב והטיפולים שונים. האבחון נשען על סיפור קליני אופייני (שריפה/חשמל, אלודיניה, נימול/חולשה), בדיקה נוירולוגית, כלי סקר ובדיקות עזר ממוקדות. בטיפול, הקו הראשון מבוסס על תרופות נוירומודולטוריות (TCA, SNRIs, גאבאפנטינוּאידים), לצד חינוך, פעילות מדורגת ונוירומודולציה לא-פולשנית במידת הצורך (Finnerup et al., 2015; Soliman et al., 2025).
טיפול כירופרקטי משתלב היטב כאשר הכאב כולל רכיב מכני־שרירי/שלדי – באמצעות התאמת עומסים, תנועה, ארגונומיה וטכניקות ידניות עדינות – כחלק ממודל רב-תחומי שמותאם למטופל הספציפי (Attal et al., 2018; Murnion, 2018). בקיצור: זיהוי מוקדם, התאמה למנגנון והשתלבות צוותית – הם המפתח להפחתת כאב, לשיפור תפקוד ולחזרה לחיים מלאים.
References:
Baskozos, G., Selvarajah, D., Purves, K., et al. (2023). Epidemiology of neuropathic pain: An analysis of UK Biobank participants. PAIN Reports, 8(2), e1052.
Colloca, L., Ludman, T., Bouhassira, D., et al. (2017). Neuropathic pain. Nature Reviews Disease Primers, 3, 17002.
Finnerup, N. B., Kuner, R., & Jensen, T. S. (2021). Neuropathic pain: From mechanisms to treatment. Physiological Reviews, 101(1), 259-301.
Finnerup, N. B., Attal, N., Haroutounian, S., et al. (2015). Pharmacotherapy for neuropathic pain in adults: A systematic review and meta-analysis. The Lancet Neurology, 14(2), 162-173.
Murnion, B. P. (2018). Neuropathic pain: Current definition and review of drug treatment. Australian Prescriber, 41(3), 60-63. https://australianprescriber.tg.org.au/articles/neuropathic-pain-current-definition-and-review-of-drug-treatment.html Australian Prescriber
Raja, S. N., Carr, D. B., Cohen, M., et al. (2020). The revised International Association for the Study of Pain definition of pain: Concepts, challenges, and compromises. PAIN, 161(9), 1976-1982.
Soliman, N., Attal, N., Finnerup, N. B., et al. (2025). Pharmacotherapy and non-invasive neuromodulation for neuropathic pain in adults: A systematic review and meta-analysis. The Lancet Neurology, 24(7), 567-589.
van Hecke, O., Torrance, N., & Smith, B. H. (2014). Neuropathic pain in the general population: A systematic review of epidemiological studies. PAIN, 155(4), 654-662.
Costigan M, Scholz J, Woolf CJ. Neuropathic pain: a maladaptive response of the nervous system to damage. Annu Rev Neurosci. 2009;32:1-32.