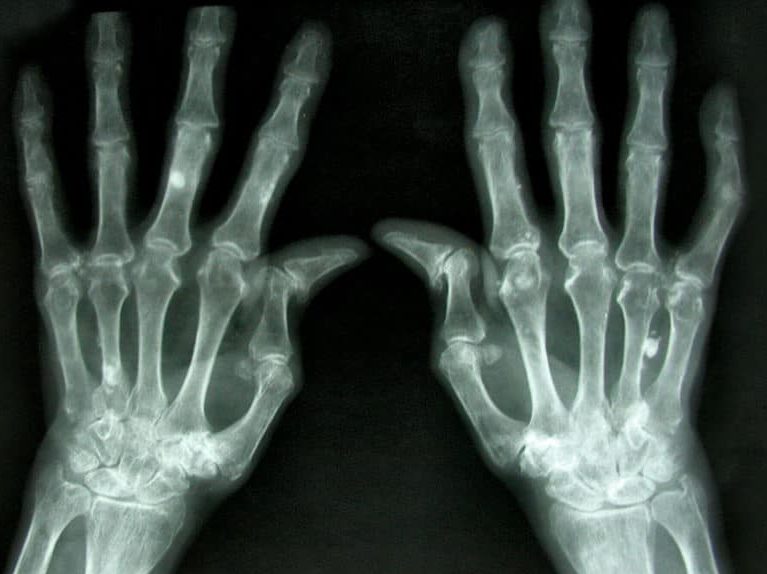
מחלות פרקים אוטואימוניות: אבחון וטיפול שוטח בפניכם מידע חשוב על הניהול הנכון של מחלות קשות אלה. המערכת החיסונית שמטרתה הגנה על בריאותינו מורכבת מסוגי תאים שונים שלהם תפקידים שונים. באופן מיטבי המערכת החיסונית לומדת במהלך החיים להכיר את מגוון האויבים שלנו ולהבחין בין אויב לידיד. זיהוי של פולש לא רצוי מפעיל את תאי הלימפוציטים מסוג B שאחראיים, לייצור נוגדנים שמטרתם תקיפתו וסילוקו של הפולש מהגוף. המערכת החיסונית מפעילה גם את תאי הלימפוציטים מסוג T שמטרתם תקיפה ישירה על הפולש.
מחלות אוטואימוניות נוצרות כאשר מסיבות שאינן ברורות המערכת החיסונית שאמורה להגן עלינו מפני וירוסים או חיידקים אלימים משתבשת. השיבוש של מערכת החיסון מוביל לכך שהיא תוקפת את התאים, הרקמות והאיברים של הגוף עצמו. בין יתר המחלות האוטואימוניות שפוגעות במפרקים נציין את דלקת מפרקים שגרונית, זאבת אדמנתית מערכתית, דלקת פרקים פסוריאטית וגם דלקת חוליות מקשחת.
מחלות אוטואימוניות הפוגעות במפרקים עלולות לגרום לכאבי גב כרוניים ונוקשות, בעיקר בבוקר, מגבלות תפקודיות ועוד. הן מתאפיינות בתקופות של הפוגה ותקופות של החמרה בסימנים והתסמינים. לא ניתן לרפא מחלת פרקים אוטואימונית אך ניתן לטפל בתסמינים שלה ולמנוע נזקים כרוניים המאפיינים אותה. אבחון מהיר ומדויק יאפשר טיפול מיטבי. במאמר "מחלות פרקים אוטואימוניות: אבחון וטיפול" נדון בנושא בהרחבה.
1) מחלות פרקים אוטואימוניות: אבחון וטיפול – רקע
מחלות אוטואימוניות (Autoimmune/Inflammatory Arthritis) הן קבוצת מצבים שבהם מערכת החיסון “משתבשת” ותוקפת רכיבים של המפרקים (ולעתים גם עור, עיניים, ריאות, כליות ומערכת העצבים). במצבה המשובש עלולה המערכת החיסונית לזהות את רקמות ותאי הגוף כפולשים בלתי רצויים ולהסתער עליהם. מחלות אוטואימוניות עלולות לפגוע בסוגים רבים של רקמות כולל מפרקים, עור שרירים מוח כלי דם ועוד ולגרום לשיבוש התפקוד שלהן. קבוצה מרכזית של מחלות אלו פוגעת במפרקים, גורמת לכאבים, נוקשות, נפיחות ואף לנזק בלתי הפיך במפרקים ולעיתים גם לאיברים נוספים.
המחלות האוטואימוניות הנפוצות במפרקים כוללות דלקת מפרקים שגרונתית (RA), זאבת (SLE), דלקת מפרקים פסוריאטית (PsA) ודלקת חוליות מקשחת (AS). אבחון מוקדם וטיפול מתאים הם קריטיים לשיפור איכות החיים ולהאטת התקדמות המחלה. מחלות אוטואימוניות שכיחות יותר אצל נשים מאשר אצל גברים ועלולות להיות להן טריגרים גנטיים וסביבתיים. במאמר "מחלות אוטואימוניות הפוגעות במפרקים: אבחון וטיפול" נרחיב בנושא.
בעשורים האחרונים חל שינוי דרמטי: מעבר מגישה של “להסתדר עם הכאב” לגישה של אבחון מוקדם וטיפול מכוון־מטרה (Treat-to-Target), עם תרופות ביולוגיות וממוקדות־מנגנון ששיפרו משמעותית את הפרוגנוזה (Smolen, 2010; Smolen, 2023).
א. המאמר מתמקד בשתי שאלות מרכזיות:
- איך מאבחנים בצורה מדויקת (ומה צריך לשלול)?
- איך בונים טיפול נכון תרופתי ולא־תרופתי כולל התייחסות זהירה ומבוססת לתפקיד האפשרי של כירופרקטיקה בתוך צוות רב־תחומי.
2) אילו מחלות נכללות תחת “מחלות פרקים אוטואימוניות”?
הקבוצה רחבה, אבל מבחינה קלינית נהוג להתמקד ב“ארתריטיס דלקתי” ובמחלות רקמת חיבור עם מעורבות מפרקים:
- דלקת מפרקים שגרונית (Rheumatoid Arthritis – RA): לרוב פוגעת במפרקים קטנים בידיים/כפות רגליים בצורה סימטרית, עם נוקשות בוקר ממושכת וסיכון לשחיקות עצם (Aletaha, 2010; Smolen, 2023).
- דלקת מפרקים פסוריאטית (Psoriatic Arthritis – PsA): קשורה לפסוריאזיס, יכולה לערב מפרקים, גידים (Enthesitis), “אצבע נקניק” (Dactylitis) ולעתים עמוד שדרה (Taylor, 2006; Gossec, 2024).
- ספונדילו־ארתריטיס צירית (Axial Spondyloarthritis – axSpA): דלקת בעיקר בעמוד השדרה והמפרקים הסקרו־איליאקיים, כאב גב דלקתי, ולעתים מעורבות עיניים/מעי (Ramiro, 2023).
- זאבת (Systemic Lupus Erythematosus – SLE): מחלה סיסטמית; כאבי/דלקות מפרקים שכיחים, לעתים ללא שחיקות קלאסיות; הטיפול נקבע לפי מעורבות איברים (Fanouriakis, 2019; Fanouriakis, 2024; Sammaritano, 2024; ACR, 2025).
- דלקות מפרקים בילדים (Juvenile Idiopathic Arthritis – JIA): קבוצה נפרדת עם עקרונות אבחון וטיפול ייחודיים (לא נעמיק כאן).
3) תסמינים שמרמזים על ארתריטיס דלקתי (ולא “שחיקה” בלבד)
יש הבדל בין כאב מכני (למשל אוסטאוארתריטיס) לבין כאב דלקתי. סימנים שמעלים חשד למחלות אוטואימוניות:
- נוקשות בוקר שנמשכת לרוב מעל 30-60 דקות
- נפיחות חמה במפרק, רגישות סביב המפרק
- שיפור עם תנועה והחמרה במנוחה (בעיקר בעמוד שדרה דלקתי)
- עייפות, חום נמוך, ירידה במשקל (לא תמיד)
תסמינים חוץ־מפרקיים: פריחה/פסוריאזיס, כיבים בפה, עיניים אדומות כואבות, שלשולים דלקתיים, תופעת ריינו, יובש משמעותי בעיניים/פה ועוד (Fanouriakis, 2019; Ramiro, 2023).
4) אבחון: איך מתקדמים נכון ומה אסור לפספס
האבחון הוא שילוב של קליניקה + בדיקות מעבדה + הדמיה, אך אין “בדיקה אחת שמוכיחה הכול”. בנוסף, יש הבדל בין קריטריוני סיווג למחקר לבין אבחנה קלינית.
3.1 אנמנזה ובדיקה גופנית (הבסיס)
רופא/ת ראומטולוג/ית מחפשים:
- דפוס פיזור מפרקים (קטנים/גדולים, סימטרי/אסימטרי)
- נוכחות סינוביטיס (דלקת מעטפת המפרק)
- נקודות חיבור גידים (Enthesitis), דקטיליטיס, טווחי תנועה, כאב גב דלקתי
- מעורבות מערכות: עור, עיניים, פה, ריאות, כליות וכו’.
3.2 בדיקות מעבדה: “לאבחן נכון, לא לנחש”
- מדדי דלקת: CRP, ESR – מועילים למעקב אך לא תמיד גבוהים.
- RA: RF ו־ACPA/anti-CCP (חיזוק חשד; לא חובה בכל חולה) (Aletaha, 2010).
- SLE: ANA (רגיש אך לא ספציפי), anti-dsDNA, anti-Sm, משלים (C3/C4), בדיקת שתן/תפקודי כליה (Fanouriakis, 2019; Fanouriakis, 2024).
- axSpA: HLA-B27 עשוי לתמוך אך לא מאבחן לבד (Ramiro, 2023).
- לפני תרופות מדכאות חיסון: סקר זיהומים (שחפת סמויה, הפטיטיס ועוד) לפי הנחיות (Fragoulis, 2023).
3.3 הדמיה: רנטגן, אולטרסאונד ו־MRI
- רנטגן: חשוב לזיהוי שחיקות/שינויים כרוניים (בעיקר RA).
- אולטרסאונד: יכול לזהות סינוביטיס וזרימת דם דלקתית, ולעזור באבחון מוקדם ובמעקב.
- MRI: שימושי במיוחד ב־axSpA לזיהוי דלקת מוקדמת במפרקים סקרו־איליאקיים לפני שינויי רנטגן (Ramiro, 2023).
3.4 קריטריוני סיווג מרכזיים (כדי להבין “איך חושבים”)
כדי להבין "איך ראומטולוג חושב", צריך להבין שהמטרה של קריטריוני הסיווג היא לאבחן מוקדם ככל האפשר כדי למנוע נזק בלתי הפיך למפרק. הנה הפירוט של השיטות המרכזיות:
דלקת מפרקים שיגרונית (RA) – קריטריוני ACR/EULAR 2010
המעבר לקריטריונים אלו ב-2010 סימן שינוי תפיסה: במקום לחכות לעיוותים במפרקים (כפי שהיה בקריטריונים הישנים), מחפשים "דלקת פעילה בשלב מוקדם".
שיטת הניקוד (ציון 6 ומעלה מתוך 10 מגדיר RA):
- מעורבות מפרקים (0-5 נקודות): ככל שיש יותר מפרקים מעורבים, ובמיוחד מפרקים קטנים (שורש כף היד, בסיס האצבעות), הניקוד עולה.
- סרולוגיה (0-3 נקודות): בדיקת נוגדנים בדם – RF (גורם ראומטואידי) ו-Anti-CCP (ספציפי מאוד ל-RA). רמות גבוהות מזכות בניקוד מקסימלי.
- מדדי דלקת (0-1 נקודות): בדיקות דם ל-CRP או ESR (שקיעת דם) גבוהות.
- משך הסימפטומים (0-1 נקודות): מעל 6 שבועות (כדי לשלול דלקות ויראליות חולפות).
דלקת מפרקים פסוריאטית (PsA) – קריטריוני CASPAR
בפסוריאזיס, האבחנה קשה יותר כי בדיקות הדם לרוב יוצאות תקינות (מחלה "סרו-נגטיבית"). לכן, שיטת CASPAR מתבססת בעיקר על ביטויים קליניים.
ציון 3 ומעלה מגדיר PsA:
- עדות לפסוריאזיס (1-2 נקודות): פסוריאזיס פעיל כרגע (2 נק'), היסטוריה אישית או משפחתית (1 נק').
- מעורבות ציפורניים (1 נקודה): שינויים אופייניים בציפורן (כמו "בורות" – Pitting).
- דקטיליטיס (1 נקודה): "אצבע נקניקייה" – נפיחות של כל האצבע ולא רק של מפרק אחד.
- שלילת RF (1 נקודה): אם בדיקת הדם ל-RF שלילית, זה מחזק את החשד ל-PsA ולא ל-RA.
- עדות רדיוגרפית (1 נקודה): סימנים לצמיחת עצם חדשה בצילום רנטגן.
אנקילוזינג ספונדיליטיס – דלקת שדרה מקשחת (axSpA) – עקרונות ועקומת הטיפול
ב-axSpA (Axial Spondyloarthritis), המוקד הוא בעמוד השדרה ובמפרקי האגן (SIJ).
איך חושבים כאן?
- כאב גב דלקתי: כאב שמופיע בלילה, משתפר בתנועה ולא במנוחה, ומלווה בקשיון בוקר ממושך.
- הדמיה: חיפוש אחר דלקת במפרקי האגן ב-MRI (בשלבים מוקדמים) או עדות לרדיוגרפיה (בשלבים מתקדמים).
4) עקרונות טיפול מודרניים: Treat-to-Target וניהול סיכונים
במחלות דלקתיות רבות, במיוחד RA ו־PsA, עיקרון המפתח הוא Treat-to-Target: קובעים יעד (הפוגה/מחלה נמוכה), מודדים פעילות מחלה באופן סדור, ומשנים טיפול אם אין שיפור משמעותי תוך חודשים ספורים (Smolen, 2010; Smolen, 2016; Smolen, 2023). המשמעות היא:
- מטרה: הגעה להפוגה מלאה (Remission) או פעילות מחלה נמוכה מאוד.
- שלב א' (Early Start): התחלה מהירה של DMARDs (תרופות משנות מהלך מחלה) כמו מתוטרקסט ב-RA.
- שלב ב' (Biologics): אם אין שיפור תוך 3-6 חודשים, עוברים לטיפולים ביולוגיים (נוגדי TNF, מעכבי IL-17 ב-PsA/axSpA, או מעכבי JAK).
- שיתוף החלטה עם המטופל/ת (Smolen, 2023; Fraenkel, 2021)
5) טיפול תרופתי: מה כולל “ארסנל” הטיפול ולמי זה מתאים?
5.1 NSAIDs (נוגדי דלקת) ו/או משככי כאב
- יעילים לשיכוך כאב ונוקשות, בעיקר ב־axSpA ובשלבים מוקדמים, אך לא משנים מהלך מחלה ברוב המצבים ולכן לרוב אינם מספיקים לבד (Ramiro, 2023).
5.2 גלוקוקורטיקואידים (סטרואידים)
יכולים “לכבות אש” במהירות, אך בגלל תופעות לוואי (אוסטאופורוזיס, סוכרת, יתר לחץ דם, זיהומים ועוד) ההמלצות המודרניות מכוונות לשימוש במינון הנמוך ביותר ולזמן הקצר ביותר, כ”גשר” עד שהטיפול הבסיסי פועל (Fraenkel, 2021; Fanouriakis, 2019).
5.3 DMARDs קונבנציונליים (csDMARDs)
ב־RA: מתוטרקסט הוא לרוב קו ראשון נפוץ, ולעיתים בשילוב תרופות נוספות לפי מצב קליני (Fraenkel, 2021; Smolen, 2023).
ב־PsA: csDMARDs עשויים לעזור בעיקר במעורבות מפרקים פריפריים, אך לעיתים יש צורך מוקדם יותר בקווים מתקדמים בהתאם לפנוטיפ (Gossec, 2024).
5.4 ביולוגיים (bDMARDs) וממוקדי־מנגנון (tsDMARDs)
כאן נמצא השיפור הגדול מאז שנות ה־2000:
- מעכבי TNF, IL-6, Abatacept, Rituximab ועוד ב־RA (Smolen, 2023; Fraenkel, 2021)
- IL-17/IL-23, TNF ועוד ב־PsA (Gossec, 2024)
- ב־axSpA: קווים ביולוגיים לפי תגובה ל־NSAIDs וחומרה, לרבות TNF ו־IL-17, עם אסטרטגיות תזמון והפחתה בהפוגה (Ramiro, 2023)
5.5 בטיחות: זיהומים, חיסונים וסקר מוקדם
ככל שמדכאים חיסון יותר – צריך לנהל סיכונים טוב יותר:
- סקר TB, הפטיטיס ועוד לפני חלק מהתרופות
- חיסונים מומלצים בהתאם להנחיות (Bass, 2023)
- הנחיות EULAR מדגישות סקר ומניעה לזיהומים כרוניים/אופורטוניסטיים באנשים עם מחלות ראומטיות אוטואימוניות המטופלים באימונוסופרסיה (Fragoulis, 2023).
5.6 נקודת עדכון חשובה: JAK inhibitors וסיכון קרדיו־אונקולוגי
מחקר בטיחות גדול הראה שבאוכלוסיית RA עם סיכון קרדיווסקולרי מוגבר, טיפול ב־tofacitinib היה קשור לסיכון גבוה יותר לאירועים קרדיווסקולריים משמעותיים ולסרטנים לעומת מעכבי TNF (Ytterberg, 2022). המשמעות אינה “לא להשתמש אף פעם”, אלא התאמת טיפול לפי פרופיל סיכון, חלופות ומעקב בהתאם להנחיות עדכניות.
6) טיפול ב־SLE עם מעורבות מפרקים (ותפיסת “בסיס לכל החולים”)
ב־SLE, מרבית ההנחיות מציינות כי הידרוקסיכלורוקווין מומלץ לרוב החולים (במינון בטוח יחסית לפי משקל ובמעקב עיניים), עם התאמות לפי פעילות המחלה ומעורבות איברים (Fanouriakis, 2019; Fanouriakis, 2024; ACR, 2025).
כאשר יש מחלה קשה/איברים (למשל כליות), קיימות המלצות ספציפיות למשטרים אימונוסופרסיביים משולבים והפחתת סטרואידים (Sammaritano, 2024; Fanouriakis, 2026).
7) טיפול לא־תרופתי: לא “בונוס”, אלא חלק מהטיפול
גם כשהתרופות עובדות, איכות חיים ותפקוד תלויים מאוד בכלים לא־תרופתיים:
7.1 פעילות גופנית ושיקום
EULAR פרסמה המלצות לפעילות גופנית לאנשים עם ארתריטיס דלקתי (RA וספונדילו־ארתריטיס) והדגישה שפעילות גופנית היא בטוחה, מועילה, וצריכה להיות מותאמת אישית (Osthoff, 2018).
הדגש הוא על:
- אימון אירובי מותאם
- חיזוק שרירים (מפחית עומס מפרקי ומשפר תפקוד)
- תרגילי טווח תנועה
- הדרכה לניהול עומסים והימנעות מ”התפרצויות עומס”
7.2 פיזיותרפיה, ריפוי בעיסוק ועזרים
סדים, התאמות ארגונומיות, טכניקות “חיסכון במפרקים”, ואימון פונקציונלי יכולים להפחית כאב ולשמר עצמאות, במיוחד במפרקי ידיים.
7.3 אורח חיים וקומורבידיות
הטיפול המודרני כולל גם:
- הפסקת עישון (קשור לחומרת RA ולתגובה לטיפול)
- ניהול משקל
- איזון סיכון קרדיווסקולרי
- שינה וסטרס (משפיעים על כאב ועייפות)
8) איפה נכנסת כירופרקטיקה במחלות פרקים אוטואימוניות?
כאן חשוב להיות מדויקים: כירופרקטיקה אינה מטפלת בשורש האוטואימוני (מערכת החיסון) ואינה מחליפה ראומטולוגיה, DMARDs או ניטור רפואי. עם זאת, כירופרקטיקה יכולה להשתלב כמרכיב תומך־תפקודי אצל חלק מהמטופלים – בדגש על כאב מכני נלווה, נוקשות, תפקוד, והדרכה – בתנאי שמכירים מגבלות ובטיחות.
8.1 מה אפשרי ומתי זה הגיוני?
- טיפול ידני עדין לרקמות רכות ומפרקים שאינם בשלב דלקתי חריף, כדי לסייע בכאב/נוקשות ולאפשר תנועה ותרגול.
- תרגול מותאם, הדרכת יציבה ועומסים, שיתוף פעולה עם פיזיותרפיה/ריפוי בעיסוק.
- תמיכה בהתנהגות בריאותית: פעילות גופנית מדורגת בהתאם להמלצות מקובלות (Osthoff, 2018).
8.2 גבולות בטיחות: יש מצבים שבהם מניפולציות מסוימות עלולות להיות מסוכנות
ב־RA, עמוד השדרה הצווארי עלול להיות מעורב עם חוסר יציבות (למשל atlanto-axial), ולכן יש הדגשה בספרות שמניפולציה צווארית במהירות גבוהה אינה מתאימה כאשר יש חשד/ממצא של חוסר יציבות (Gillick, 2015). גם דיווחים ודיונים קליניים מדגישים צורך בהקשר ובזהירות, ובהבחנה בין אזורים מעורבים/דלקתיים לבין אזורים שאינם מעורבים (Chung, 2015).
לכן, שילוב כירופרקטי נכון חייב לכלול:
- סקר סימני אזהרה (נוירולוגיים, צוואריים, דלקת חריפה)
- תיאום עם ראומטולוג/ית כשיש מחלה פעילה, טיפול אימונוסופרסיבי משמעותי או חשד למעורבות צווארית
- העדפה של גישות תרגוליות וטכניקות עדינות על פני “התאמות” אגרסיביות במצבים רגישים.
8.3 השורה התחתונה
כירופרקטיקה יכולה להיות כלי עזר לשיפור תפקוד וניהול כאב כחלק מטיפול משולב, אבל לא תחליף לטיפול מבוסס־ראיות שמדכא דלקת ומונע נזק מפרקי.
9) מעקב, יעדים ומדדי הצלחה: איך יודעים שהטיפול עובד?
בגישה מודרנית, הצלחה נמדדת לא רק בכאב אלא גם ב:
- ירידה במדדי פעילות מחלה (לפי מחלה ספציפית)
- שיפור בתפקוד יומיומי, עייפות ואיכות חיים
- מניעת נזק מבני בהדמיה
- הפחתת סטרואידים לאורך זמן
- ניהול סיכונים: זיהומים, בריאות עצם, חיסונים, קרדיווסקולרי (Smolen, 2023; Fraenkel, 2021; Fragoulis, 2023)
10) מתי חשוב לפנות בדחיפות?
- עין אדומה כואבת עם טשטוש ראייה (חשד לאובאיטיס)
- כאב גב דלקתי עם חום/ירידה במשקל לא מוסברת
- קוצר נשימה חדש, כאב חזה, נפיחות ברגל אחת (תסחיף/דלקת ריאות/סיבוכים)
- חולשה או נימול מתקדמים (חשד מעורבות עצבית/צווארית)
- ירידה חדה בתפקוד כלייתי/דם בשתן ב־SLE (Fanouriakis, 2019; Sammaritano, 2024)
סיכום
מחלות פרקים אוטואימוניות הן מצבים כרוניים אך כיום ברי־שליטה הרבה יותר בזכות אבחון מוקדם, Treat-to-Target, ותרופות ביולוגיות/ממוקדות. האבחון נשען על דפוס קליני, בדיקות מעבדה והדמיה, תוך אבחנה מבדלת זהירה. הטיפול האפקטיבי הוא משולב: תרופות שמדכאות דלקת ומונעות נזק + פעילות גופנית ושיקום + ניהול סיכונים (חיסונים, סקר זיהומים, פרופיל לבבי). כירופרקטיקה יכולה להשתלב כתמיכה תפקודית וניהול כאב – בזהירות, תוך הכרה במגבלות, ובהימנעות ממניפולציות מסוכנות במצבים כמו מעורבות צווארית ב־RA.
References:
Aletaha, D., Neogi, T., Silman, A. J., Funovits, J., Felson, D. T., Bingham, C. O., III, Birnbaum, N. S., Burmester, G. R., Bykerk, V. P., Cohen, M. D., Combe, B., Costenbader, K. H., Dougados, M., Emery, P., Ferraccioli, G., Hazes, J. M. W., Hobbs, K., Huizinga, T. W. J., Kavanaugh, A., … Hawker, G. (2010). 2010 Rheumatoid arthritis classification criteria: An American College of Rheumatology/European League Against Rheumatism collaborative initiative. Annals of the Rheumatic Diseases, 69(9), 1580-1588.
Bass, A. R., Bridges, S. L., Jr., Burke, L., Dubrovsky, A., Fischer, A., et al. (2023). 2022 American College of Rheumatology guideline for vaccinations in patients with rheumatic and musculoskeletal diseases. Arthritis & Rheumatology, 75(3), 449-464.
Fanouriakis, A., Kostopoulou, M., Alunno, A., Aringer, M., Bajema, I., Boletis, J. N., Cervera, R., et al. (2019). 2019 update of the EULAR recommendations for the management of systemic lupus erythematosus. Annals of the Rheumatic Diseases, 78(6), 736-745.
Fanouriakis, A., Aringer, M., Bajema, I., Berden, J., Boletis, J., et al. (2024). EULAR recommendations for the management of systemic lupus erythematosus: 2023 update. Annals of the Rheumatic Diseases, 83(1), 15-27.
Fanouriakis, A., Aringer, M., Bajema, I., Berden, J., Boletis, J., et al. (2026). EULAR recommendations for the management of lupus nephritis: 2025 update. Annals of the Rheumatic Diseases. (Advance online publication).
Fragoulis, G. E., Nikiphorou, E., Dey, M., et al. (2023). 2022 EULAR recommendations for screening and prophylaxis of chronic and opportunistic infections in adults with autoimmune inflammatory rheumatic diseases. Annals of the Rheumatic Diseases, 82(6), 742-753.
Fraenkel, L., Bathon, J. M., England, B. R., St. Clair, E. W., Arayssi, T., et al. (2021). 2021 American College of Rheumatology guideline for the treatment of rheumatoid arthritis. Arthritis & Rheumatology, 73(7), 1108-1123.
Gillick, J. L., Wainwright, J., & Das, K. (2015). Rheumatoid arthritis and the cervical spine: A review on the role of surgery. BioMed Research International, 2015, 252456.
Gossec, L., Smolen, J. S., Ramiro, S., et al. (2024). EULAR recommendations for the management of psoriatic arthritis with pharmacological therapies: 2023 update. Annals of the Rheumatic Diseases, 83(6), 706-719.
Osthoff, A. K. R., Niedermann, K., Braun, J., Adams, J., Brodin, N., Dagfinrud, H., et al. (2018). 2018 EULAR recommendations for physical activity in people with inflammatory arthritis and osteoarthritis. Annals of the Rheumatic Diseases, 77(9), 1251-1260.
Ramiro, S., Nikiphorou, E., Sepriano, A., Ortolan, A., Webers, C., Baraliakos, X., Landewé, R., van der Heijde, D., & ASAS-EULAR Task Force. (2023). ASAS-EULAR recommendations for the management of axial spondyloarthritis: 2022 update. Annals of the Rheumatic Diseases, 82(1), 19-34.
Sammaritano, L. R., Rovin, B. H., Adler, S., et al. (2024). 2024 American College of Rheumatology guideline for the management of lupus nephritis. Arthritis & Rheumatology. (Advance online publication).
Smolen, J. S., Aletaha, D., Bijlsma, J. W. J., Breedveld, F. C., Boumpas, D., et al. (2010). Treating rheumatoid arthritis to target: Recommendations of an international task force. Annals of the Rheumatic Diseases, 69(4), 631-637.
Smolen, J. S., Breedveld, F. C., Burmester, G. R., Bykerk, V., Dougados, M., et al. (2016). Treating rheumatoid arthritis to target: 2014 update of the recommendations of an international task force. Annals of the Rheumatic Diseases, 75(1), 3-15.
Smolen, J. S., Landewé, R., Bijlsma, J., Burmester, G. R., Dougados, M., et al. (2023). EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2022 update. Annals of the Rheumatic Diseases, 82(1), 3-18.
Taylor, W., Gladman, D., Helliwell, P., Marchesoni, A., Mease, P., & Mielants, H. (2006). Classification criteria for psoriatic arthritis: Development of new criteria from a large international study. Arthritis & Rheumatism, 54(8), 2665-2673.
Ytterberg, S. R., Bhatt, D. L., Mikuls, T. R., Koch, G. G., Fleischmann, R., Rivas, J. L., Germino, R., Menon, S., Sun, Y., Wang, C., & Winthrop, K. L. (2022). Cardiovascular and cancer risk with tofacitinib in rheumatoid arthritis. The New England Journal of Medicine, 386(4), 316-326.
American College of Rheumatology. (2025). 2025 American College of Rheumatology guideline for the treatment of systemic lupus erythematosus. Arthritis & Rheumatology.